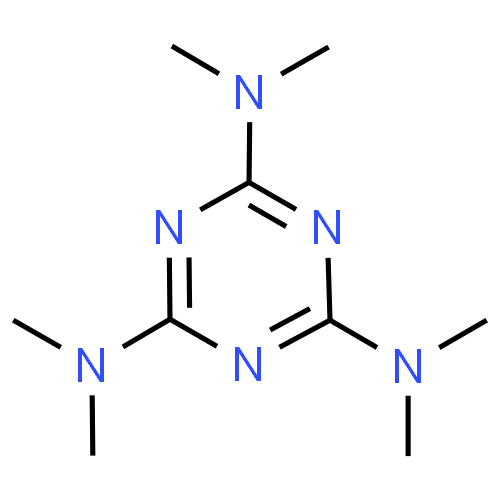
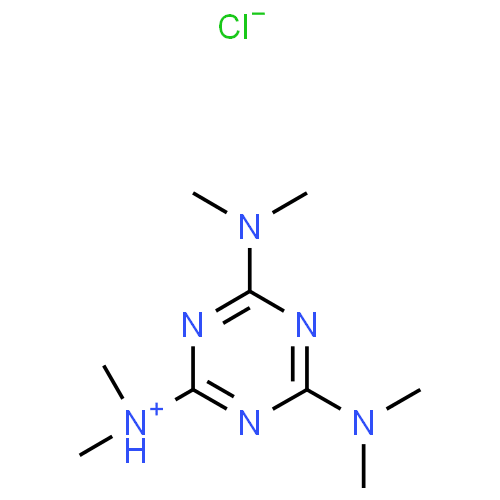
Pharmacocinétique - ALTRÉTAMINE - voie orale
Absorption
La cinétique de l'altrétamine a été déterminée chez des patientes présentant un cancer de l'ovaire avancé. Après administration orale de doses de 120 à 300 mg/m2 les pics plasmatiques sont atteints entre 0.5 et 4 heures.
Distribution
Les concentrations maximales atteintes ne sont pas proportionnelles à la dose administrée et varient de 0.2 à 20.8 mg/l.
L'altrétamine et ses métabolites, pentaméthylmélamine et tétraméthylmélamine, se lient respectivement à 94%, 75% et 50% aux protéines plasmatiques.
L'altrétamine se concentre essentiellement dans les tissus à composante lipidique.
Biotransformation
L'altrétamine est métabolisée par les cytochromes P450 essentiellement en dérivés N-methylé éliminés par le rein.
Élimination
Le temps de demi-vie d'élimination est compris entre 2.3 et 10.2 heures.
Après administration orale de 14C altrétamine (4 mg/kg), chez 2 patients, on a constaté que le pic de radioactivité se situe à 1 heure après l'administration et que la demi-vie d'élimination plasmatique est d'environ 13 heures. On retrouve 61% de la radioactivité administrée dans les urines de 24 heures et 89% dans les urines de 72 heures. 48 heures après l'administration on retrouve 0.1 % dans les fèces.
Dosage - ALTRÉTAMINE - voie orale
Gélule
La dose totale quotidienne doit être répartie en 2 à 3 prises données après les repas et avant le coucher.
En fonction de l'indication, de l'état du malade et des renseignements fournis par la surveillance hématologique et clinique, les posologies moyennes sont les suivantes :
En monothérapie, la dose habituelle est de 260 mg/m2 par jour, pendant 14 à 21 jours consécutifs. A répéter tous les 28 jours.
En cas d'association, la dose indiquée en monothérapie peut être diminuée en fonction de l'association avec un ou plusieurs cytostatiques ou cytolytiques, habituellement 150 mg/m2/j pendant 8 à 14 jours. A répéter tous les 28 jours.
Population pédiatrique
Mode d'administration
Voie orale
Indications - ALTRÉTAMINE - usage systémique
ALTRÉTAMINE est indiqué en traitement de 2ème ligne du cancer de l'ovaire et du cancer bronchique à petites cellules.
Ce médicament est contre-indiqué en cas de :
Grossesse et allaitement.
Hypersensibilité ou intolérance au gluten, en raison de la présence d'amidon de blé (gluten).
Association avec le vaccin contre la fièvre jaune .
Association avec la phénytoïne à visée prophylactique .
Effets indésirables - ALTRÉTAMINE - usage systémique
Toxicité hématologique habituellement modérée : thrombopénie, granulopénie, anémie.
Toxicité neurologique possible (en cas de traitement prolongé), mais réversible : neuropathies périphériques sensitives et motrices, manifestations centrales (confusion, agitation, dépression, hallucination),
Intolérance digestive à type de nausées, vomissements, perte d'appétit, et occasionnellement diarrhée,
Réactions cutanées possibles (rash, prurit, lésions eczémateuses),
Cystites,
Aménorrhée, azoospermie.
Jusqu'à présent, aucun cas de surdosage aigu n'a été rapporté. En cas de surdosage, on doit s'attendre à une exagération des effets secondaires. On pratiquera quotidiennement une numération formule sanguine pour guider d'éventuels gestes symptomatiques.
Grossesse
Les études effectuées chez l'animal ont mis en évidence un effet tératogène.
En clinique, il n'existe pas actuellement de données suffisamment pertinentes pour évaluer un éventuel effet malformatif ou ftotoxique de ALTRÉTAMINE lorsqu'il est administré pendant la grossesse.
Ce médicament est contre-indiqué au cours de la grossesse.
Allaitement
Le passage dans le lait maternel de l'altrétamine n'est pas connu. En raison de la possible toxicité de ce médicament pour le nouveau-né allaité, l'allaitement est contre-indiqué en cas de traitement de la mère par ALTRÉTAMINE.
Associations contre-indiquées
+ Phénytoïne à visée prophylactique décrit pour doxorubicine, daunorubicine, carboplatine, cisplatine, carmustine, vincristine, vinblastine, bléomycine, méthotrexate :
Risque de survenue de convulsions par diminution de l'absorption digestive de la phénytoïne par le cytotoxique.
+ Vaccin antiamarile :
Risque de maladie vaccinale généralisée mortelle.
Associations déconseillées
+ Vaccins vivants atténués (sauf fièvre jaune) :
Risque de maladie généralisée éventuellement mortelle. Ce risque est majoré chez les sujets déjà immunodéprimés par la maladie sous-jacente. Utiliser un vaccin inactivé lorsqu'il existe (poliomyélite).
Selon des données cliniques limitées, il n'est pas recommandé d'utiliser conjointement l'altrétamine avec la pyridoxine, en raison d'un risque de diminution de l'efficacité du cytotoxique et ce, malgré une diminution de sa neurotoxicité.
Associations faisant l'objet de précautions d'emploi
+ Phénytoïne, en cas de traitement antérieur à la chimiothérapie décrit pour doxorubicine, daunorubicine, carboplatine, cisplatine, carmustine, vincristine, vinblastine, bléomycine, méthotrexate :
Risque de survenue de convulsions par diminution de l'absorption digestive de la phénytoïne par le cytotoxique. Associer momentanément une benzodiazépine anticonvulsivante.
Associations à prendre en compte
+ Ciclosporine (et, par extrapolation, tacrolimus) décrit pour doxorubicine, étoposide :
Immunodépression excessive avec risque de lymphoprolifération.
Communes à tous les cytotoxiques :
Anticoagulants oraux : en raison de l'augmentation du risque thrombotique lors des affections tumorales, le recours à un traitement anticoagulant est fréquent. La grande variabilité intra-individuelle de la coagulabilité au cours de ces affections, à laquelle s'ajoute l'éventualité d'une interaction entre les anticoagulants oraux et la chimiothérapie anticancéreuse imposent, s'il est décidé de traiter le patient par anticoagulants oraux, d'augmenter la fréquence des contrôles de l'INR.

 Français
Français Русский
Русский