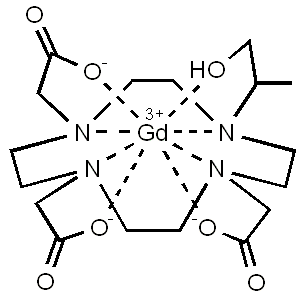
Le gadotéridol est un produit de contraste, paramagnétique, non ionique, utilisé dans l'imagerie par résonance magnétique.
Le gadotéridol placé dans un champ magnétique diminue les temps de relaxation longitudinaux dans les régions ciblées. Aux doses recommandées, cet effet est particulièrement sensible dans des séquences pondérées par les temps de relaxation T1.
osmolalité = 630 mOsm/kg
viscosité à 20°C = 2 mPa.s
Pharmacocinétique - GADOTÉRIDOL - usage parentéral
La distribution du GADOTÉRIDOL répond à un modèle bicompartimental ouvert. Injecté par voie intraveineuse, le gadotéridol se répartit dans le système vasculaire et l'espace interstitiel.
Les demi-vies de distribution et d'élimination sont respectivement de 0,2 ± 0,04 et 1,57 ± 0,08 heure. Le gadotéridol est exclusivement éliminé par le rein, avec une excrétion de 94,4 ± 4,8 %, dans les 24 heures suivant l'injection.
Il n'a pas été mis en évidence de biodégradation du gadotéridol ni de relargage de gadolinium libre in vivo.
Dosage - GADOTÉRIDOL - usage parentéral
Solution injectable
La dose la plus faible permettant un rehaussement de contraste suffisant à des fins diagnostiques doit être utilisée. La dose recommandée chez l'adulte et l'enfant est de 0,1 mmol/kg de la solution 0,5 mmol/mL (0,2 mL/kg).
Dans quelques cas exceptionnels, comme la confirmation du caractère unique d'une métastase ou la détection de tumeurs leptoméningées, une deuxième injection de 0,2 mmol/kg peut être administrée.
Populations particulières :
Insuffisants rénaux
GADOTÉRIDOL ne doit être administré aux patients présentant une insuffisance rénale sévère (DFG < 30 mL/min/1,73 m2) et en période périopératoire de transplantation hépatique qu'après une évaluation approfondie du rapport bénéfice/risque et que si les informations diagnostiques sont indispensables et ne peuvent être obtenues au moyen d'une IRM sans rehaussement du contraste . S'il est nécessaire d'administrer GADOTÉRIDOL, la dose ne doit pas excéder 0,1 mmol/kg de masse corporelle. Ne pas administrer plus d'une dose au cours de l'examen IRM. En raison du manque d'information sur les administrations répétées, les injections de GADOTÉRIDOL ne doivent pas être réitérées, sauf si l'intervalle entre les injections est d'au moins sept jours.
Nouveau-nés jusqu'à l'âge de 4 semaines et nourrissons jusqu'à l'âge d'un an
En raison de l'immaturité de la fonction rénale chez le nouveau-né jusqu'à l'âge de 4 semaines et chez le nourrisson jusqu'à l'âge d'un an, GADOTÉRIDOL ne doit être utilisé chez ces patients qu'après une évaluation attentive et à une dose n'excédant pas 0,1 mmol/kg de masse corporelle. Ne pas administrer plus d'une dose au cours de l'examen. En raison du manque d'information sur les administrations répétées, les injections de GADOTÉRIDOL ne doivent pas être réitérées, sauf si l'intervalle entre les injections est d'au moins sept jours.
La réalisation d'une IRM du corps entier n'est pas recommandée chez le nourrisson âgé de moins de 6 mois.
Sujets âgés (à partir de 65 ans)
Aucune adaptation posologique n'est nécessaire. Utiliser avec prudence chez les sujets âgés .
Mode d'administration
GADOTÉRIDOL est utilisé en voie intraveineuse et en utilisation monodose.
Afin de garantir l'administration de la dose prescrite, l'injection devra être suivie d'un embole de 5 mL de solution injectable de chlorure de sodium 9 g/L.
L'examen devra être réalisé dans l'heure qui suit l'injection.
Indications - GADOTÉRIDOL - usage systémique
Ce médicament est à usage diagnostique uniquement.
GADOTÉRIDOL est indiqué chez l'adulte et l'enfant de tout âge pour le :
Rehaussement du contraste en Imagerie par Résonance Magnétique (IRM) des territoires crâniens, rachidiens et médulaires.
GADOTÉRIDOL peut également être utilisé pour l'Imagerie par Résonance Magnétique des pathologies du corps entier.
Il permet la visualisation de structures anatomiques ou des lésions anormales et aide à la différenciation entre les tissus sains et pathologiques.
GADOTÉRIDOL ne doit être utilisé que lorsque le diagnostic est nécessaire et que ce diagnostic ne peut pas être obtenu par imagerie par résonance magnétique (IRM) sans rehaussement de contraste.
Contre-indications liées à la technique IRM.
Effets indésirables - GADOTÉRIDOL - usage systémique
Au cours des études cliniques sur 2827 patients, 6,3 % des patients ont présenté un effet indésirable lié à l'administration de GADOTÉRIDOL
Les effets indésirables liés à l'utilisation de GADOTÉRIDOL sont généralement d'intensité légère à modérée, et de nature transitoire
Les effets indésirables les plus fréquemment rencontrés lors de l'administration de GADOTÉRIDOL depuis sa commercialisation sont les nausées.
Les réactions d'hypersensibilité les plus fréquemment observées sont les réactions cutanées, qui peuvent être localisées, étendues ou généralisées. Ces réactions sont le plus souvent de survenue immédiate (durant l'injection ou dans l'heure qui suit le début de l'injection) ou parfois retardée (une heure à quelques jours après l'injection).
Les réactions immédiates peuvent comprendre un ou plusieurs types de manifestations cutanées, respiratoires et/ou cardiovasculaires, survenant de façon concomitante ou successive. Chacun de ces signes peuvent annoncer un état de choc qui n'évolue que rarement vers un décès.
Des cas isolés de fibrose néphrogénique systémique (FNS) ont été rapportés avec GADOTÉRIDOL, le plus souvent chez des patients ayant également reçu d'autres produits de contraste contenant du gadolinium .
Les effets indésirables sont présentés dans le tableau ci-dessous par Système Organe Classe et par fréquence en utilisant les catégories suivantes : très fréquent (³ 1/10), fréquent (³1/100 à 1<1/10), peu fréquent (³1/1 000 à 1<1/100), rare (³1/10 000 à <1/1 000), très rare (<1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Système Organe Classe | Fréquence : effet indésirable |
Affections du système immunitaire | Rare : réaction anaphylactique * |
Affections psychiatriques | Rare : anxiété |
Affections du système nerveux | Peu fréquent : céphalées, sensation vertigineuse, paresthésie, dysgueusie Rare : convulsion, coordination anormale, altération mentale Fréquence indéterminée : coma, réaction vasovagale **, perte de connaissance |
Affections oculaires | Peu fréquent : augmentation de la sécrétion lacrymale |
Affections de l'oreille et du labyrinthe | Rare : acouphènes |
Affections cardiaques | Peu fréquent : accélération de la fréquence cardiaque Rare : troubles du rythme nodal Fréquence indéterminée : arrêt cardiaque |
Affections vasculaires | Peu fréquent : hypotension, vasodilatation |
Affections respiratoires, thoraciques et médiastinales | Rare : laryngospasme, dyspnée, toux, rhinite, apnée, sibilances Fréquence indéterminée : arrêt respiratoire, dème pulmonaire |
Affections gastro-intestinales | Fréquent : nausée Peu fréquent : vomissement, bouche sèche Rare : diarrhée, douleur abdominale, dème de la langue, prurit oral, gingivite |
Affections de la peau et du tissu sous-cutané | Peu fréquent : prurit, urticaire, rash Rare : dème de la face Fréquence indéterminée : fibrose systémique néphrogénique, angioedème |
Affections musculo-squelettiques et systémiques | Rare : raideur musculaire |
Affections du rein et des voies urinaires | Fréquence indéterminée : insuffisance rénale aiguë*** |
Troubles généraux et anomalies au site d'administration | Peu fréquent : douleur au point d'injection, réaction au site de l'injection (notamment due à l'extravasation du produit de contraste), asthénie Rare : fièvre, douleur thoracique |
* Réactions anaphylactiques :
Comme avec les autres chélates de gadolinium, des cas de réactions anaphylactiques/ d'hypersensibilité ont été rapportés avec GADOTÉRIDOL. Ces réactions peuvent présenter divers niveaux de gravité incluant le choc anaphylactique voire le décès. Les effets indésirables ont concerné un ou plusieurs systèmes d'organes. Dans la plupart des cas, il s'agissait des systèmes respiratoires, cardiovasculaires et/ou cutanéo-muqueux. Les symptômes communément rapportés incluent: rétrécissement de la gorge, irritation de la gorge, dyspnée, inconfort dans la poitrine, sensation de chaleur, dysphagie, sensation de brûlure, dème du pharynx ou du larynx et hypotension.
**Réactions vasovagales
Des réactions vasovagales, allant rarement jusqu'à la syncope vasovagale, ont été rapportées au cours ou immédiatement après l'administration de GADOTÉRIDOL. Cet état est fréquemment lié à un trouble émotionnel ou à des stimuli douloureux/déplaisants (ex : piqûre de l'aiguille lors de la mise en place de l'intraveineuse). Les symptômes fréquemment rapportés incluent: nausées, vertiges et diaphorèse.
Dans des cas graves, pouvant aller jusqu'à la syncope, les patients sont habituellement pâles et diaphorétiques et présentent une altération de leur état de conscience ainsi qu'une bradycardie. De plus, il est fréquent que les patients présentent appréhension, agitation, faiblesse et hypersécrétion salivaire. Lors du diagnostic, il est impératif de distinguer ce type de réaction d'une réaction d'hypersensibilité afin de prendre les mesures thérapeutiques appropriées contre la stimulation vagale.
***Insuffisance rénale aigüe
Des cas d'insuffisance rénale aiguë ont été rapportés chez les patients souffrant d'une insuffisance rénale préexistante.
Population pédiatrique
La fréquence, la nature et la sévérité des effets indésirables chez l'enfant sont similaires à ceux observées chez l'adulte. Néanmoins les données ne proviennent que d'une seule étude pédiatrique ayant porté sur 103 enfants de 6 mois à 20 ans.
Aucun surdosage n'a été rapporté.
En cas de très forte dose, la perte hydrique et électrolytique doit être compensée par une réhydratation appropriée. La fonction rénale doit être surveillée pendant au moins trois jours.
GADOTÉRIDOL peut être éliminé de l'organisme par hémodialyse. Toutefois, il n'est pas démontré que l'hémodialyse soit appropriée dans la prévention de la fibrose néphrogénique systémique (FNS).
Grossesse
Il n'existe pas de données sur l'utilisation du gadotéridol chez la femme enceinte. Les études effectuées chez l'animal n'ont pas mis en évidence d'effets délétères directs ou indirects sur la reproduction . GADOTÉRIDOL ne doit pas être utilisé pendant la grossesse. Seuls les examens absolument nécessaires devraient être effectués pendant la grossesse, lorsque le bénéfice probable dépasse largement le risque pour la mère et le ftus.
Allaitement
Les produits de contraste contenant du gadolinium sont excrétés dans le lait maternel en très petites quantités . Aux doses cliniques, aucun effet n'est prévu chez le nourrisson allaité en raison de la petite quantité excrétée dans le lait et de la faible absorption intestinale. Le médecin et la mère allaitante doivent décider s'il faut poursuivre l'allaitement ou le suspendre pendant les 24 heures suivant l'administration de GADOTÉRIDOL
Associations à prendre en compte
+ Bêta-bloquants, substances vasoactives, inhibiteurs de l'enzyme de conversion de l'angiotensine, antagonistes des récepteurs de l'angiotensine :
Ces médicaments entraînent une baisse de l'efficacité des mécanismes de compensation cardiovasculaire des troubles tensionnels: le médecin doit en être informé avant l'injection de complexe de gadolinium et disposer des moyens de réanimation.

 Français
Français Русский
Русский