Pharmacodynamique
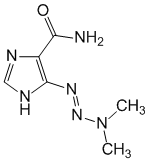
La dacarbazine est un imidazole diméthyltriazène ayant une action reproductible chez les patients atteints de mélanome métastatique. La structure de la dacarbazine a une ressemblance frappante avec celle du métabolite amino-5 imidazole-4 carboxamide (AIC) qui est transformé en acide inosinique par les enzymes participant à la synthèse des bases puriques.
Il a d'abord été supposé qu'elle agissait comme anti-métabolite, en inhibant le métabolisme purique et la synthèse des acides nucléiques. Toutefois, la similarité des structures est peu pertinente puisque la dacarbazine est considérablement métabolisée dans le foie par le système du cytochrome P450 par réaction de N-déméthylation. Le dérivé monométhyl se divise ensuite spontanément pour donner le métabolite AIC et un composé intermédiaire, probablement le diazométhane, qui se décompose pour former un ion méthyl-carbonium. Cet ion se fixe sur les groupes nucléophiles des acides nucléiques et d'autres macromolécules, agissant ainsi comme alkylant. La position 7 de la guanine sur l'ADN est particulièrement sensible à l'alkylation.
On pense que la dacarbazine agit comme alkylant chez l'homme. Elle interfère dans la synthèse de l'ADN, de l'ARN et des protéines mais sa cytotoxicité ne concerne pas une phase spécifique du cycle cellulaire. En général, elle est le plus efficace dans l'inhibition de la synthèse de l'ARN. La dacarbazine détruit lentement les cellules et il n'a pas été observé d'action immunodépressive chez l'homme. Il n'existe pas d'études systémiques des effets dose-réponse mais un rapport isolé suggère que des doses majorées pourraient augmenter les chances de réponse.
La dacarbazine subit une photodégradation spontanée à la lumière et se décompose en 5-diazoimidazole-4-carboxamide et en diméthylamine. Le 5-diazoimidazole-4-carboxamide peut attaquer les groupes nucléophiles de l'ADN et subit également une réorganisation structurelle pour former de la 2-azahypoxanthine. Toutefois, les produits de la photodégradation de la dacarbazine ne contribuent probablement pas beaucoup à sa cytotoxicité, bien qu'ils jouent probablement un rôle dans la douleur locale à type de brûlure après injection par voie intraveineuse et dans les réactions systémiques associées au médicament.
Pharmacocinétique
Pharmacocinétique - DACARBAZINE - usage parentéral
La décroissance plasmatique est rapide: demi-vie de distribution de 3 minutes et demi-vie d'élimination de 40 minutes.
Le volume de distribution est de 0,6 l/kg.
La clairance totale du produit est de 15,4 ml/kg/min, alors que la clairance rénale est de 7 ml/kg/min (50% de la dose IV est retrouvée dans les urines).
Les aires sous la courbe sont comparables quel que soit le schéma d'administration.
Le métabolite AIC apparaît dans le plasma dès la fin de l'injection en bolus et atteint un pic en 15 minutes. Sa demi-vie d'élimination est d'environ 75 minutes avec une clairance rénale d'environ 4 ml/kg/min.
Dosage
Dosage - DACARBAZINE - usage parentéral
Poudre pour solution injectable ou pour perfusion
Le traitement par DACARBAZINE doit être administré exclusivement par des médecins expérimentés dans les domaines respectifs de l'oncologie ou de l'hématologie.
Pendant le traitement par DACARBAZINE, de fréquents contrôles des numérations sanguines ainsi qu'une surveillance des fonctions hépatique et rénale sont nécessaires. Les réactions gastro-intestinales sévères étant fréquentes, il est conseillé de recourir à des antiémétiques et des mesures de prise en charge symptomatique.
Des troubles gastro-intestinaux et hématologiques sévères pouvant survenir, une analyse extrêmement soigneuse du rapport bénéfice/risque doit être réalisée avant chaque cure de traitement par la dacarbazine.
La prise d'aliments avant l'administration de DACARBAZINE doit être évitée afin de limiter la sévérité des nausées et vomissements. Les excréta et vomissures doivent être manipulés avec précaution.
Les posologies suivantes pourront être utilisées. Pour plus de précisions, voir la littérature scientifique actuelle.
Mélanome malin
La dacarbazine peut être administrée seule à des doses de 200 à 250 mg/m2 de surface corporelle/jour par voie intraveineuse pendant 5 jours toutes les 3 semaines.
La dacarbazine peut être administrée en perfusion courte (sur 20 30 minutes).
Il est également possible d'administrer 850 mg/m2 de surface corporelle en jour 1 puis une fois toutes les 3 semaines en perfusion intraveineuse.
Maladie de Hodgkin
La dacarbazine doit être administrée par voie intraveineuse à la dose quotidienne de 375 mg/m2 de surface corporelle tous les 15 jours en association avec la doxorubicine, la bléomycine et la vinblastine (protocole ABVD).
Sarcome des tissus mous
Pour traiter le sarcome des tissus mous chez l'adulte, la dacarbazine doit être administrée par voie intraveineuse à des doses quotidiennes de 250 mg/m2 de surface corporelle (jours 1 à 5) en association avec la doxorubicine toutes les 3 semaines (protocole ADIC).
Durée du traitement
Le médecin traitant devra décider de la durée du traitement au cas par cas en tenant compte du type et du stade de la maladie sous-jacente, de la polythérapie utilisée, de la réponse à la dacarbazine et de ses effets indésirables.
Dans le cas de la maladie de Hodgkin à un stade avancé, il est habituellement recommandé d'administrer 6 cycles de polythérapie ABVD.
Dans le cas du mélanome malin métastasé et du sarcome des tissus mous à un stade avancé, la durée du traitement dépend de l'efficacité et de la tolérance chez chaque patient.
Populations particulières
Patients présentant une insuffisance rénale/hépatique :
En présence d'une insuffisance rénale ou hépatique légère à modérée isolée, il n'est habituellement pas nécessaire de réduire la dose. Chez les patients atteints d'insuffisances rénale et hépatique combinées, l'élimination de la dacarbazine est plus lente. Cependant, aucune recommandation validée concernant la réduction de la dose ne peut actuellement être fournie.
Patients âgés :
L'expérience disponible chez les patients âgés étant limitée, aucune instruction particulière ne peut être fournie concernant l'utilisation du médicament chez ces patients.
Population pédiatrique
La sécurité et l'efficacité de DACARBAZINE chez les enfants et les adolescents n'ont pas encore été établies.
Mode d'administration
Précautions à prendre avant la manipulation ou l'administration du médicament :
La dacarbazine est sensible à la lumière. Les solutions reconstituées doivent être tenues à l'abri de la lumière, y compris pendant l'administration (matériel de perfusion opaque).
Lors de l'administration, l'injection paraveineuse du médicament doit être soigneusement évitée car cela pourrait entraîner des douleurs localisées et des lésions tissulaires.
En cas d'injection paraveineuse, l'administration doit être immédiatement interrompue et le reste de la dose, le cas échéant, doit être injecté dans une autre veine.
Débit de perfusion :
Les doses comprises entre 200 et 850 mg/m2 de surface corporelle doivent être administrées en perfusion intraveineuse sur une durée de 20 à 30 minutes.
Il est recommandé de tester d'abord la perméabilité de la veine à l'aide de 5 à 10 mL de solution isotonique de chlorure de sodium ou de glucose à 5 %. Le même type de solution devra être utilisé après la perfusion pour purger les résidus de médicament dans la tubulure de perfusion.
La solution reconstituée est limpide et jaune pâle. La solution pour perfusion diluée est limpide et pratiquement incolore.
Indications
Indications - DACARBAZINE - usage systémique
La dacarbazine est indiquée dans le traitement du mélanome malin métastatique.
Les autres indications de la dacarbazine dans le cadre d'une chimiothérapie d'association sont :
Maladie de Hodgkin.
Sarcome des tissus mous de l'adulte à un stade avancé (sauf mésothéliome et sarcome de Kaposi).
Contre-indications
Ce médicament est CONTRE-INDIQUÉ dans les cas suivants :
Patients ayant présenté une hypersensibilité connue à la dacarbazine.
Patients atteints d'une maladie hépatique ou rénale grave.
Grossesse ou allaitement.
En association avec le vaccin contre la fièvre jaune, avec l'usage prophylactique de la phénytoïne ou avec des vaccins vivants atténués .
Effets indésirables
Effets indésirables - DACARBAZINE - usage systémique
Les fréquences sont définies selon les conventions suivantes : très fréquent (> 1/10), fréquent (> 1/100, ≤ 1/10), peu fréquent (> 1/1000, ≤ 1/100), rare (> 1/10 000, ≤ 1/1000), très rare (≤ 1/10 000), non connu (estimation impossible à partir des données disponibles).
Affections du sang et du système lymphatique | Fréquents |
| Anémie, leucopénie, thrombocytopénie, |
| insuffisance médullaire |
Troubles du système immunitaire | Très rare |
| Anaphylaxie, réactions allergiques |
Troubles métaboliques et nutritionnels | Fréquent |
| Anorexie |
Troubles psychiatriques | Peu fréquents |
| Confusion |
Trouble du système nerveux | Peu fréquents |
| Céphalées, crises épileptiques, paresthésies |
| faciales, léthargie. |
Troubles oculaires | Peu fréquents |
| Vision trouble. |
Troubles vasculaires | Peu fréquents |
| Rougeur du visage. |
Troubles gastro-intestinaux | Fréquents |
| Nausées, vomissements. |
| Rares |
| Diarrhées. |
Troubles hépatobiliaires | Peu fréquents |
| Elévation des transaminases (AST, ALT), |
| augmentation des phosphatases alcalines, |
| augmentations de la lactate deshydrogénase. |
| (LDH). |
| Toxicité hépatique, thrombose des veines. |
| hépatiques, nécrose hépatique, Syndrome de |
| Budd-Chiari éventuellement fatal. |
Troubles cutanés et des tissus sous-cutanés | Peu fréquent |
| Alopécie, rash passager. |
| Rare |
| Photosensibilité. |
| Très rare |
| Erythème, urticaire, exanthème maculo-papuleux. |
Troubles rénaux et urinaires | Peu fréquent |
| Insuffisance rénale avec élévation de la |
| créatinémie et de l'urémie. |
Troubles généraux et touchant le site | Peu fréquents |
d'administration | Syndrome pseudogrippal, malaise. |
| Rare |
| Irritation au site d'injection. |
Affections du sang et du système lymphatique :
Aplasie médullaire, leucopénie, thrombocytopénie et anémie . Les conséquences cliniques de la leucopénie peuvent être de la fièvre, des infections et une septicémie.
Troubles gastro-intestinaux :
Les symptômes d'anorexie, de nausée, de vomissement sont les effets secondaires les plus fréquents.
Les vomissements peuvent durer de 1 à 12 heures. Il est rare que des nausées ou des vomissements rebelles nécessitent l'interruption du traitement.
Troubles hépatobiliaires :
Elévation des transaminases (AST, ALT), des phosphatases alcalines, de la LDH. Généralement, les taux redeviennent normaux dans les deux semaines.
Troubles généraux et touchant le site d'administration :
Dans des cas peu fréquents, des patients ont présenté un syndrome pseudogrippal avec fièvre, myalgie et malaise. Ce syndrome survient généralement après de fortes doses uniques, environ sept jours après le traitement par la dacarbazine, dure de 7 à 21 jours et peut réapparaître lors des traitements successifs. On pense que l'irritation veineuse et que certaines réactions indésirables générales sont la conséquence de la formation des produits de photo-dégradation.
Surdosage
Les principales complications auxquelles on peut s'attendre en cas de surdosage sont l'insuffisance médullaire grave, éventuellement l'aplasie médullaire dont l'apparition peut prendre jusqu'à deux semaines.
Le délai de survenue du nadir des leucocytes et des thrombocytes peut atteindre 4 semaines. Même si l'on craint seulement un surdosage, une surveillance stricte et de longue durée des numérations sanguines est essentielle et des traitements adjuvants, comme des transfusions appropriées dans le cas d'insuffisance médullaire, peuvent être nécessaires. On ne connaît pas d'antidote au surdosage de dacarbazine. Il convient donc d'être particulièrement prudent pour éviter un surdosage de ce médicament.
Grossesse/Allaitement
Grossesse
Le potentiel mutagène, tératogène et cancérogène de la dacarbazine a été démontré chez l'animal. Il convient donc de considérer qu'il existe un risque accru d'effets tératogènes chez l'être humain. On ignore si la dacarbazine franchit la barrière placentaire et passe dans le lait maternel.
Femmes en âge de procréer
Les femmes en âge de procréer doivent utiliser des méthodes de contraception efficaces.
Hommes traités par la dacarbazine
Il est conseillé aux hommes de prendre des mesures contraceptives pendant le traitement et pendant 6 mois après l'arrêt du traitement.
Interactions avec d'autres médicaments
Interactions communes à tous les cytotoxiques :
+ Anticoagulants oraux
En raison de l'augmentation du risque thrombotique lors des affections tumorales, le recours à un traitement anticoagulant est fréquent. La grande variabilité intra-individuelle de la coagulabilité au cours de ces affections, à laquelle s'ajoute l'éventualité d'une interaction entre les anticoagulants oraux et la chimiothérapie anticancéreuse imposent, s'il est décidé de traiter le patient par anticoagulants oraux, d'augmenter la fréquence des contrôles de l'INR.
Associations contre-indiquées
+ Vaccin antiamarile
Risque de maladie vaccinale généralisée mortelle.
Associations déconseillées
+ Phénytoïne (et, par extrapolation, fosphénytoïne)
Risque de survenue de convulsion par diminution de l'absorption digestive de la seule phénytoïne par le cytotoxique, ou bien risque de majoration de la toxicité, ou de perte d'efficacité du cytotoxique par augmentation de son métabolisme hépatique par la phénytoïne ou la fosphénytoïne.
+ Vaccins vivants atténués (sauf antiamarile)
Risque de maladie vaccinale généralisée éventuellement mortelle.
Ce risque est majoré chez les sujets déjà immunodéprimés par la maladie sous-jacente.
Utiliser un vaccin inactivé lorsqu'il existe (poliomyélite).
Associations à prendre en compte
+ Immunosuppresseurs
Immunodépression excessive avec risque de syndrome lymphoprolifératif.
Interactions liées à la dacarbazine :
Associations faisant l'objet de précautions d'emploi
+ Fotémustine
Avec la dacarbazine à doses élevées : risque de toxicité pulmonaire (syndrome de détresse respiratoire aiguë de l'adulte).
Ne pas utiliser simultanément mais respecter un délai d'une semaine entre la dernière administration de fotémustine et le premier jour de la cure de dacarbazine.

 Français
Français Русский
Русский