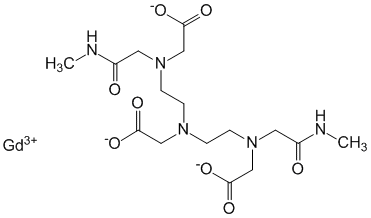
Pharmacodynamique
Le
gadodiamide est un produit de contraste, paramagnétique, utilisé dans l'imagerie par résonance magnétique.
Le gadodiamide placé dans un champ magnétique diminue les temps de relaxation longitudinaux dans les régions ciblées. Aux doses recommandées, cet effet est particulièrement sensible dans des séquences pondérées par les temps de relaxation T1.
- Osmolalité (mOsm/kg H2O) à 37°C
780
- Viscosité (mPa-s) à 20°C
..2,8
- Viscosité (mPa-s) à 37°C
..1,9
- Densité à 20°C (kg/L)
..1,15
- Relaxivité molaire
r1 (mM-1 s-1) à 10 MHz et 37° C
4,6
r2 (mM-1 s-1) à 10 MHz et 37°C
.5,1
- pH
..6,0-7,0
Le gadodiamide est facilement soluble dans l'eau.
Pharmacocinétique
Pharmacocinétique - GADODIAMIDE - usage parentéral
Injecté par voie intraveineuse, le gadodiamide se répartit dans le système vasculaire et l'espace interstitiel.
Chez les patients à fonction rénale normale, les demi-vies de distribution et d'élimination sont respectivement de 3,6 ± 3 minutes et 78 ± 15 minutes. Le gadodiamide est exclusivement éliminé par le rein, avec une excrétion de 95 à 98 %, 24 heures après injection.
En cas d'insuffisance rénale (débit de filtration glomérulaire < 30 mL/min) l'augmentation de la demi-vie d'élimination est, dans une certaine mesure, inversement proportionnelle au débit de filtration glomérulaire. La substance est dialysable.
Il n'a pas été mis en évidence de biodégradation du gadodiamide ni de relargage de gadolinium libre in vivo.
Dosage
Dosage - GADODIAMIDE - usage parentéral
Solution injectable
La dose recommandée chez l'adulte, l'enfant et le nourrisson est de 0,2 mL/kg (0,1 mmol/kg).
Dans quelques cas exceptionnels comme la confirmation du caractère unique d'une métastase ou la détection de tumeurs leptoméningées, une deuxième injection de 0,4 mL/kg (0,2 mmol/kg) peut être administrée.
Injection intraveineuse stricte.
Afin de garantir une injection totale du produit de contraste, l'injection devra être suivie d'un bolus de 5 mL de solution injectable de chlorure de sodium 9g/L.
L'examen devra être réalisé dans les 45 minutes suivant l'injection. L'amélioration optimale du contraste est généralement observée dans les premières minutes suivant l'administration du produit.
En angiographie lorsque les résultats de l'examen en cours le rendent nécessaire, il est possible de renouveler le produit de contraste avec un maximum de 3 injections successives d'une dose simple.
Populations particulières
Insuffisance rénale
GADODIAMIDE est contre-indiqué chez les patients présentant une insuffisance rénale sévère (clairance estimée de la créatinine < 30 mL/min/1,73 m2) et chez les patients durant la période pré ou post-opératoire d'une transplantation hépatique .
GADODIAMIDE ne doit être utilisé chez les patients présentant une insuffisance rénale modérée (clairance estimée de la créatinine entre 30 et 59 mL/min/1,73 m²) à une dose n'excédant pas 0,1 mmol/kg de poids corporel qu'après une évaluation attentive du rapport bénéfice/risque .
Ne pas administrer plus d'une dose au cours de l'examen IRM.
En raison du manque d'information sur les administrations répétées, les injections d'GADODIAMIDE ne doivent pas être réitérées sauf si l'intervalle entre les injections est d'au moins 7 jours.
Nouveau-nés âgés de 4 semaines ou moins et nourrissons âgés de 1 an ou moins
GADODIAMIDE est contre-indiqué chez les nouveau-nés âgés de 4 semaines ou moins .
En raison de l'immaturité de la fonction rénale des nourrissons âgés de 1 an ou moins, GADODIAMIDE ne doit être utilisé chez ces patients qu'après une évaluation attentive et à une dose n'excédant pas 0,1 mmol/kg de poids corporel.
Lors d'un examen d'IRM, il n'est pas possible d'utiliser plus d'une dose.
En raison du manque d'information sur les administrations répétées, les injections d'GADODIAMIDE ne doivent pas être réitérées sauf si l'intervalle entre les injections est d'au moins 7 jours.
Patients âgés (65 ans et plus)
Aucune adaptation de posologie n'est nécessaire. Utiliser avec prudence chez les sujets âgés .
Indications
Indications - GADODIAMIDE - usage systémique
Ce médicament est à usage diagnostique uniquement.
Imagerie par résonance magnétique nucléaire :
Flacon de 5 mL, 10 mL, 15 mL et 20 mL :
- pathologies cérébrales et médullaires
- pathologies du rachis
- autres pathologies du corps entier (dont celles nécessitant une exploration par angiographie).
Flacons de 40 mL et 50 mL :
- exploration vasculaire (angiographie)
Contre-indications
Contre-indications liées à la technique IRM.
GADODIAMIDE est contre-indiqué chez les patients présentant une insuffisance rénale sévère (clairance estimée de la créatinine < 30 mL/min/1,73 m2), chez les patients durant la période pré ou post-opératoire d'une transplantation hépatique et chez les nouveau-nés âgés de 4 semaines ou moins .
Effets indésirables
Effets indésirables - GADODIAMIDE - usage systémique
Au cours des études cliniques sur 459 patients, 6 % des patients ont présenté un effet indésirable lié à l'administration d'GADODIAMIDE.
Les effets indésirables liés à l'utilisation d'GADODIAMIDE sont généralement d'intensité légère à modérée, et de nature transitoire.
Les effets indésirables les plus fréquemment rencontrés lors de l'administration d'GADODIAMIDE depuis sa commercialisation sont : les réactions d'hypersensibilité, les nausées et les vomissements.
Lors des réactions d'hypersensibilité, les effets les plus fréquemment observés sont les effets cutanés, qui peuvent être localisés, étendus ou généralisés. Ces réactions sont le plus souvent de survenue immédiate (durant l'injection ou dans l'heure qui suit le début de l'injection) ou parfois retardée (une heure à quelques jours après l'injection), et se présentent alors sous forme de réactions cutanées.
Les réactions immédiates regroupent un ou plusieurs effets, d'apparition concomitante ou successive incluant le plus souvent des manifestations cutanées, respiratoires et/ou cardiovasculaires, qui peuvent chacun être annonciateurs d'un état de choc débutant et aller très rarement jusqu'au décès.
Des cas de fibrose néphrogénique systémique (FNS) ont été rapportés avec GADODIAMIDE .
Les effets indésirables sont présentés dans le tableau ci-dessous par Système Organe Classe et par fréquence en utilisant les catégories suivantes : très fréquent (³ 1/10), fréquent (³1/100 à <1/10), peu fréquent (³1/1 000 à <1/100), rare (³1/10 000 à <1/1 000), très rare (<1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
Système Organe Classe | Fréquence : effet indésirable |
Affections hématologiques et du système lymphatique | Fréquence indéterminée : hémolyse |
Affections du système immunitaire | Peu fréquent : hypersensibilité Fréquence indéterminée : réaction anaphylactique, réaction anaphylactoïde |
Affections du système nerveux | Fréquent : céphalées, Peu fréquent : sensation vertigineuse, paresthésie, dysgueusie Fréquence indéterminée : coma |
Affections cardiaques | Fréquence indéterminée : arrêt cardiaque, tachycardie |
Affections vasculaires | Fréquence indéterminée : hypotension |
Affections respiratoires, thoraciques et médiastinales | Rare : dyspnée, toux Fréquence indéterminée : arrêt respiratoire, bronchospasme, éternuement, dème pulmonaire, laryngospasme, asthme, congestion nasale, gorge sèche |
Affections gastro-intestinales | Fréquent : nausée, Peu fréquent : vomissement, diarrhée Rare : douleur abdominale |
Affections de la peau et du tissu sous-cutané | Peu fréquent : prurit, Rare : urticaire, rash, érythème hyperhidrose, Fréquence indéterminée : eczéma, fibrose systémique néphrogénique, plaque cutanée* |
Affections musculo-squelettiques et systémiques | Fréquence indéterminée : dorsalgie |
Affections du rein et des voies urinaires | Rare : Insuffisance rénale aigüe, Fréquence indéterminée : Augmentation de la créatininémie |
Troubles généraux et anomalies au site d'administration | Fréquent : sensation de chaud, sensation de froid, Rare : douleur au point d'injection, réaction au site de l'injection, extravasation au point d'injection, gêne au niveau du site d'injection, inflammation au point d'injection en cas d'extravasation, dème de la face, Fréquence indéterminée : nécrose au point d'injection en cas d'extravasation |
Investigations | Fréquence indéterminée : fer sérique augmenté, bilirubinémie augmentée, ferritinémie augmentée |
* Des cas de plaques cutanées associées au gadolinium avec corps sclérotiques mis en évidence en histologie ont été rapportés avec le gadodiamide chez des patients ne présentant pas par ailleurs de signes ou symptômes de fibrose néphrogénique systémique.
Les effets indésirables suivants ont été rapportés avec d'autres produits de contraste intraveineux à base de gadolinium. Ils sont donc susceptibles de survenir également au cours d'un traitement avec GADODIAMIDE :
Système Organe Classe | Effet indésirable |
Affections psychiatriques | agitation, anxiété, confusion |
Affections du système nerveux | présyncope, syncope, convulsion, parosmie, tremblement |
Affections oculaires | vision trouble, conjonctivite, augmentation de la sécrétion lacrymale, hyperémie oculaire, cécité transitoire, douleur oculaire |
Affections de l'oreille et du labyrinthe | acouphènes, douleur auriculaire |
Affections cardiaques | bradycardie, arythmie, palpitations |
Affections vasculaires | hypertension, pâleur, vasodilatation |
Affections gastro-intestinales | hypersécrétion salivaire, bouche sèche, distension abdominale, flatulence |
Affections de la peau et du tissu sous-cutané | dermite bulleuse |
Affections musculo-squelettiques et systémiques | contractures musculaires, faiblesse musculaire |
Affections du rein et des voies urinaires | incontinence urinaire, nécrose tubulaire rénale, insuffisance rénale aigüe |
Troubles généraux et anomalies au site d'administration | malaise, douleur thoracique, fièvre, frissons,asthénie, gêne thoracique |
Investigations | prolongation PR de l'électrocardiogramme, épreuve de la fonction hépatique anormale |
Effets indésirables chez l'enfant
La fréquence, la nature et la gravité des effets indésirables attendus chez les enfants sont les mêmes que chez l'adulte.
Surdosage
Aucun surdosage n'a été rapporté.
En cas de très forte dose, la perte hydrique et électrolytique doit être compensée par une réhydratation appropriée. La fonction rénale doit être surveillée pendant au moins trois jours.
GADODIAMIDE peut être éliminé par hémodialyse. Toutefois, il n'est pas démontré que l'hémodialyse soit appropriée dans la prévention de la fibrose néphrogénique systémique (FNS).
Grossesse/Allaitement
Grossesse
Il n'existe pas de données sur l'utilisation de
gadodiamide chez la femme enceinte. Des études effectuées chez l'animal après des doses élevées et répétées ont mis en évidence une toxicité sur la reproduction . GADODIAMIDE ne doit pas être utilisé pendant la grossesse à moins que la situation clinique de la patiente ne justifie l'utilisation de gadodiamide.
Allaitement
On ne sait pas si le gadodiamide est excrété dans le lait maternel. Un risque pour le nouveau-né ne peut être exclu. L'allaitement doit être interrompu pendant au moins 24 heures après l'administration d'GADODIAMIDE.
Interactions avec d'autres médicaments
Avec la méthode colorimétrique utilisant l'orthocrysophtaline (OCP), il y a une sous-estimation de la calcémie.
Associations à prendre en compte
Bêta-bloquants, substances vasoactives, inhibiteurs de l'enzyme de conversion de l'angiotensine, antagonistes des récepteurs de l'angiotensine : ces médicaments entraînent une baisse de l'efficacité des mécanismes de compensation cardiovasculaire des troubles tensionnels : le médecin doit en être informé avant l'injection de complexe de gadolinium et disposer des moyens de réanimation.

 Français
Français Русский
Русский