Pharmacodynamique
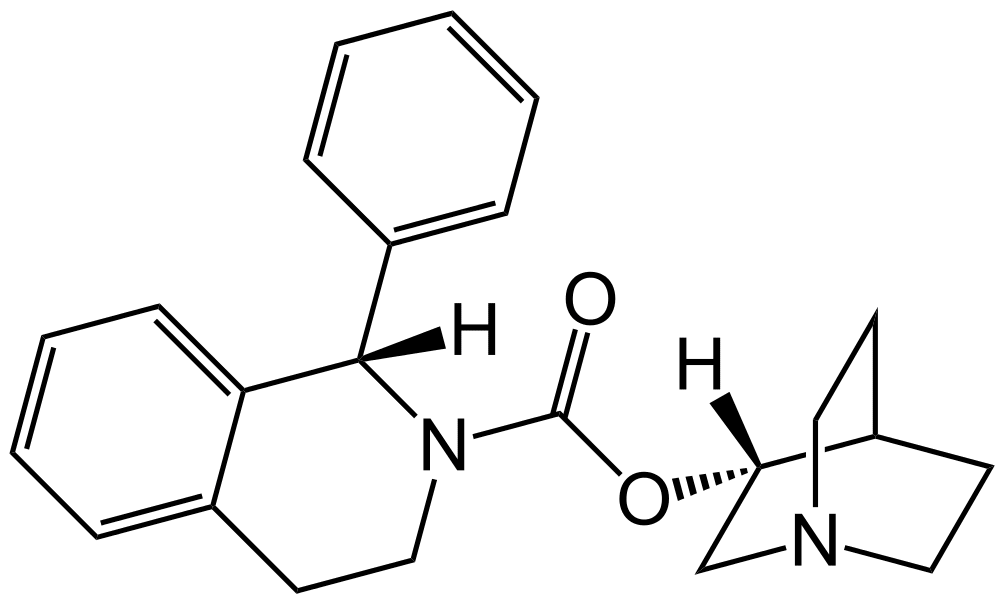
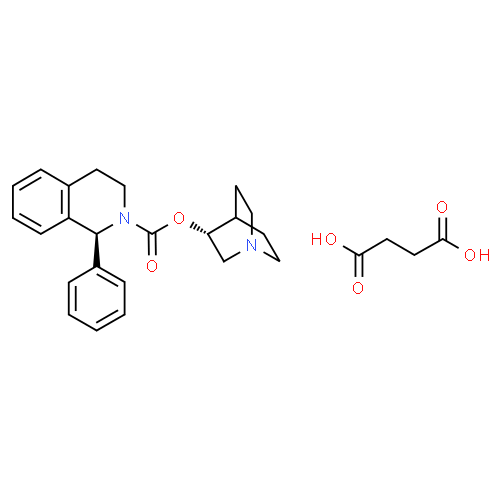
La solifénacine est un antagoniste compétitif spécifique des récepteurs cholinergiques.
La vessie est innervée par des nerfs parasympathiques cholinergiques. L'acétylcholine contracte le détrusor, muscle lisse, en agissant sur les récepteurs muscariniques, principalement sur leur sous-type M3. Des études pharmacologiques in vitro et in vivo ont montré que la solifénacine était un inhibiteur compétitif des récepteurs muscariniques appartenant au sous-type M3. De plus, la solifénacine a une activité antagoniste spécifique sur les récepteurs muscariniques, son affinité pour d'autres récepteurs et canaux ioniques étudiés étant faible ou nulle.
Pharmacocinétique
Pharmacocinétique - SOLIFÉNACINE - voie orale
Absorption
Après la prise des comprimés de SOLIFÉNACINE , les concentrations plasmatiques maximales de solifénacine (Cmax) sont atteintes au bout de3 à 8 heures. La valeur de tmax est indépendante de la dose. La valeur de Cmax et celle de l'aire sous la courbe (ASC) augmentent proportionnellement à la dose dans la fourchette de doses allant de 5 à 40 mg. La biodisponibilité absolue est d'environ 90%.
La prise d'aliments ne modifie pas la concentration maximale ni l'ASC de la solifénacine.
Distribution
Après administration intraveineuse, le volume apparent de distribution de la solifénacine est d'environ 600 litres. La solifénacine est fortement (environ 98%) liée aux protéines plasmatiques, essentiellement à l'α1-glycoprotéine acide.
Biotransformation
La solifénacine est largement métabolisée dans le foie, essentiellement par l'iso-enzyme 3A4 du cytochrome P450 (CYP3A4). Il existe cependant d'autres voies métaboliques qui peuvent contribuer au métabolisme de la solifénacine. La clairance systémique de la solifénacine est d'environ 9,5 L/h et la demi-vie d'élimination de la solifénacine est de 45 à 68 heures. Après administration orale, un métabolite pharmacologiquement actif (4R-hydroxy solifénacine) et trois métabolites inactifs (N-glycuronide, N-oxyde et 4R-hydroxy-N-oxyde de solifénacine) ont été identifiés dans le plasma, en plus de la solifénacine.
Elimination
Après une administration unique de 10 mg de solifénacine marquée par le 14C, on a retrouvé environ 70% de la radioactivité dans les urines et 23% dans les selles en l'espace de 26 jours. Dans les urines, environ 11% de la radioactivité sont retrouvés sous forme de substance active inchangée ; environ 18% sous la forme du métabolite N-oxyde, 9% sous la forme du métabolite 4R-hydroxy-N-oxyde et 8% sous la forme du métabolite 4R-hydroxy (métabolite actif).
Linéarité/non-linéarité
La pharmacocinétique est linéaire dans la fourchette des doses thérapeutiques.
Autres populations particulières
Personnes âgées
Aucun ajustement posologique n'est nécessaire en fonction de l'âge. Des études ont montré qu'après l'administration de succinate de solifénacine (5 mg et 10 mg une fois par jour), l'exposition à la solifénacine (exprimée par l'ASC) était comparable chez les sujets âgés en bonne santé (entre 65 et 80 ans) et les sujets jeunes en bonne santé (moins de 55 ans). Chez les personnes âgées, la vitesse moyenne d'absorption, exprimée par le tmax, était légèrement plus lente et la demi-vie d'élimination était augmentée d'environ 20%.Ces différences, peu importantes, ont été considérées comme cliniquement négligeables.
La pharmacocinétique de la solifénacine n'a pas été étudiée chez l'enfant et l'adolescent.
Sexe
La pharmacocinétique de la solifénacine n'est pas modifiée par le sexe.
Appartenance ethnique La pharmacocinétique de la solifénacine n'est pas modifiée par la race. Insuffisance rénale
Chez des patients souffrant d'insuffisance rénale légère à modérée, l'ASC et la Cmax de la solifénacine ne sont pas significativement différentes de celles observées chez des sujets sains.
Chez des patients souffrant d'insuffisance rénale sévère (clairance de la créatinine ≤ 30 mL/min), l'exposition à la solifénacine était significativement plus importante que chez les témoins, avec des augmentations de Cmax d'environ 30%, de l'ASC de plus de 100% et de t½ de plus de 60%. Il existe une relation statistiquement significative entre la clairance de la créatinine et la clairance de la solifénacine.
La pharmacocinétique de la solifénacine n'a pas été étudiée chez les patients hémodialysés.
Insuffisance hépatique
En cas d'insuffisance hépatique modérée (score de Child-Plugh de 7 à 9), la valeur de Cmax est inchangée, l'AUC augmente de 60% et t½ est doublée. La pharmacocinétique de la solifénacine n'a pas été étudiée chez des patients souffrant d'insuffisance hépatique sévère.
Dosage
Dosage - SOLIFÉNACINE - voie orale
Comprimé pelliculé
Adultes, y compris personnes âgées
La posologie recommandée est de 5 mg de succinate de solifénacine une fois par jour.
Si nécessaire, la dose peut être augmentée à 10 mg de succinate de solifénacine une fois par jour.
Population pédiatrique
La sécurité et l'efficacité de SOLIFÉNACINE chez les enfants n'ont pas encore été établies, SOLIFÉNACINE ne doit pas être prescrit chez l'enfant.
Insuffisance rénale
Aucun ajustement posologique n'est nécessaire en cas d'insuffisance rénale légère à modérée (clairance de la créatinine > 30 mL/min).
Insuffisance hépatique
Aucun ajustement posologique n'est nécessaire en cas d'insuffisance hépatique légère.
Puissants inhibiteurs de l'iso-enzyme 3A4 du cytochrome P450
Mode d'administration
Le comprimé de SOLIFÉNACINE 5 mg doit être pris par voie orale et avalé entier avec de l'eau, sans le croquer. Le médicament peut être pris indifféremment pendant ou en dehors des repas.
Hyperactivité vésicale
Adultes, y compris personnes âgées
La posologie recommandée est de 5 mg (5 ml) de succinate de solifénacine une fois par jour.
Si nécessaire, la dose peut être augmentée à 10 mg (10 ml) de succinate de solifénacine une fois par jour.
Population pédiatrique
L'efficacité de SOLIFÉNACINE chez les enfants et les adolescents souffrant d'hyperactivité vésicale n'a pas été établie. Par conséquent, SOLIFÉNACINE ne doit pas être utilisé pour le traitement de l'hyperactivité vésicale chez l'enfant et l'adolescent de moins de 18 ans.
Hyperactivité détrusorienne neurogène
Population pédiatrique (agée de 2 à 18 ans)
La posologie recommandée de SOLIFÉNACINE , suspension buvable est déterminée sur la base du poids du patient. Le traitement doit être débuté à la posologie initiale recommandée. Par la suite, la posologie peut être augmentée jusqu'à la dose minimale efficace. La dose maximale ne doit pas être dépassée. Au cours du traitement à long terme, les patients doivent être évalués périodiquement pour la poursuite du traitement et pour un ajustement posologique potentiel, au moins une fois par an ou plus fréquemment, si indiqué. Les doses à administrer en fonction du poids corporel du patient sont mentionnées dans le tableau ci-dessous.
Intervalle de poids (kg) Dose initiale (ml) §1 Dose maximale (ml) §2
Intervalle de poids (kg) | Dose initiale (ml) §1 | Dose maximale (ml) §2 |
9 à 15 | 2 | 4 |
> 15 à 30 | 3 | 5 |
> 30 à 45 | 3 | 6 |
> 45 à 60 | 4 | 8 |
> 60 | 5 | 10 |
§ La formulation de SOLIFÉNACINE en suspension buvable a une concentration de 1 mg/ml.
1 Correspondant à l'exposition à l'état d'équilibre après l'administration d'une dose quotidienne de 5 mg chez les adultes
2 Correspondant à l'exposition à l'état d'équilibre après l'administration d'une dose quotidienne de 10 mg chez les adultes
SOLIFÉNACINE , suspension buvable doit être pris une fois par jour par voie orale.
SOLIFÉNACINE , suspension buvable ne doit pas être utilisé chez les enfants âgés de moins de 2 ans.
Insuffisance rénale
Aucun ajustement posologique n'est nécessaire en cas d'insuffisance rénale légère à modérée (clairance de la créatinine > 30 ml/min). En cas d'insuffisance rénale sévère (clairance de la créatinine ≤ 30 ml/min), le traitement doit être utilisé avec prudence et la dose de 5 mg (5 ml) une fois par jour (adultes) ou la dose initiale (enfants et adolescents) ne doit pas être dépassée .
Insuffisance hépatique
Aucun ajustement posologique n'est nécessaire en cas d'insuffisance hépatique légère. En cas d'insuffisance hépatique modérée (score de Child-Pugh de 7 à 9), le traitement doit être utilisé avec prudence et la dose de 5 mg (5 ml) une fois par jour (adultes) ou la dose initiale (enfants et adolescents) ne doit pas être dépassée .
Puissants inhibiteurs de l'iso-enzyme 3A4 du cytochrome P450
La dose maximale de SOLIFÉNACINE , suspension buvable doit être limitée à 5 mg (5 ml) (adultes) ou à la dose initiale (enfants et adolescents) en cas d'administration concomitante de kétoconazole ou d'un autre puissant inhibiteur de l'iso-enzyme CYP3A4 utilisé à des doses thérapeutiques ; par exemple le ritonavir, le nelfinavir, l'itraconazole .
Mode d'administration
SOLIFÉNACINE , suspension buvable doit être pris par voie orale et suivi d'un verre d'eau. Il ne doit pas être ingéré en même temps que des aliments et/ou d'autres boissons.
La prise concomitante avec des aliments et/ou des boissons peut causer une libération de la solifénacine dans la bouche causant un goût amer et un engourdissement de la bouche.
Une seringue pour prise orale adaptée et un adaptateur doivent être utilisés afin de mesurer la dose exacte .
Indications
Indications - SOLIFÉNACINE - usage systémique
Traitement symptomatique de l'incontinence urinaire par impériosité et/ou de la pollakiurie et de l'impériosité urinaire pouvant s'observer chez les patients souffrant d'hyperactivité vésicale.
Contre-indications
La solifénacine est contre-indiquée :
Chez les patients souffrant de rétention urinaire, d'une affection gastro-intestinale sévère (dont le mégacôlon toxique), de myasthénie ou d'un glaucome par fermeture de l'angle, ainsi que chez les patients à risque vis-à-vis de ces affections ;
Effets indésirables
Effets indésirables - SOLIFÉNACINE - usage systémique
Résumé du profil de tolérance
Compte tenu de l'effet pharmacologique de la solifénacine, SOLIFÉNACINE 5 mg peut provoquer des effets indésirables de type anticholinergique, de sévérité légère à modérée et dont la fréquence est dose dépendante.
L'effet indésirable le plus fréquemment rapporté sous SOLIFÉNACINE 5 mg est la sécheresse de la bouche. Elle a été observée chez 11% des patients traités par 5 mg une fois par jour, 22% des patients traités par 10 mg une fois par jour et 4% des patients sous placebo. La sécheresse de la bouche était généralement d'intensité légère et n'a qu'occasionnellement entraîné l'interruption du traitement. En général, l'observance du traitement était très élevée (environ 99%) et environ 90% des patients traités par SOLIFÉNACINE 5 mg ont poursuivi leur traitement jusqu'à la fin des études (12 semaines).
Liste tabulée des effets indésirables
| Système d'organes, (classification MedDRA) | Très fréquent≥ 1/10 | Fréquent≥ 1/100, < 1/10 | Peu fréquent≥ 1/1 000, < 1/100 | Rare≥ 1/10 000, < 1/1 000 | Très rare< 1/10 000 | Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) |
| Infections et infestations | | | Infection urinaire, Cystite | | | |
| Affections du système immunitaire | | | | | | Réaction anaphylactique* |
| Troubles du métabolisme et de la nutrition | | | | | | Diminution de l'appétit* Hyperkaliémie* |
| Affections psychiatriques | | | | | Hallucinations* Etats confusionnels* | Délire* |
| Affections du système nerveux | | | Somnolence Dysgueusie | Etourdissement*, Céphalées* | | |
| Affections oculaires | | Vision floue | Sécheresse oculaire | | | Glaucome* |
| Affections cardiaques | | | | | | Torsade de pointes* Allongement de l'intervalle QT à l'électrocardiogramme* Fibrillation auriculaire* Palpitations* Tachycardie* |
| Affections respiratoires, thoraciques et médiastinales | | | Sécheresse nasale | | | Dysphonie* |
| Affections gastro-intestinales | Sécheresse buccale | Constipation Nausées Dyspepsie Douleur abdominale | Reflux gastro-sophagien Sécheresse de la gorge | Occlusion colique Fécalome Vomissements* | | Iléus* Gêne abdominale* |
| Affections hépatobiliaires | | | | | | Troubles hépatiques* Anomalies des tests de la fonction hépatique* |
| Affections de la peau et du tissu sous-cutané | | | Sécheresse de la peau | Prurit*, Erythème*, | Erythème polymorphe* Urticaire* Angioedème* | Dermatite exfoliative* |
| Affections musculo-squelettiques et systémiques | | | | | | Faiblesse musculaire* |
| Affections du rein et des voies urinaires | | | Troubles mictionnels | Rétention d'urine | | Insuffisance rénale* |
| Troubles généraux et anomalies au site d'administration | | | Fatigue dème périphérique | | | |
* observé après commercialisation
Surdosage
Symptômes
Un surdosage avec le succinate de solifénacine peut potentiellement aboutir à des effets anticholinergiques sévères. Une dose maximale de 280 mg de succinate de solifénacine suite à une administration accidentelle chez un seul patient sur une période de 5 heures, a abouti à des troubles des fonctions supérieures n'entrainant pas d'hospitalisation.
Traitement
En cas de surdosage en succinate de solifénacine, utiliser du charbon activé. Un lavage d'estomac est utile s'il est effectué dans l'heure, mais ne pas provoquer de vomissements.
Comme pour les autres anticholinergiques, les symptômes peuvent être traités comme suit :
Effets anticholinergiques centraux sévères tels qu'hallucinations ou excitation importante : par la physostigmine ou le carbachol ;
Convulsions ou excitation importante : par des benzodiazépines ;
Insuffisance respiratoire : par ventilation artificielle ;
Tachycardie : par des bêta-bloquants ;
Rétention d'urines : par sondage ;
Mydriase : par un collyre de pilocarpine et/ou placer le patient dans une pièce sombre.
Comme avec les autres antimuscariniques, en cas de surdosage, une surveillance spécifique est nécessaire chez les patients présentant un risque de prolongation de QT (par exemple en cas d'hypokaliémie, de bradycardie et de traitement concomitant par des médicaments prolongeant l'intervalle QT) ou ayant une cardiopathie préexistante significative (par exemple une ischémie myocardique, des troubles du rythme, une insuffisance cardiaque congestive).
Grossesse/Allaitement
Grossesse
Il n'existe pas de données cliniques concernant des patientes ayant débuté une grossesse sous traitement par la solifénacine. Les expérimentations animales n'ont pas montré d'effets nocifs directs sur la fertilité, le développement embryonnaire/ftal ou la mise bas . Le risque éventuel chez la femme est inconnu. La solifénacine doit être prescrite avec prudence chez la femme enceinte.
Allaitement
Il n'existe pas de données concernant l'excrétion de la solifénacine dans le lait maternel. Chez la souris, la solifénacine et/ou ses métabolites ont été excrétés dans le lait et ont entraîné des anomalies du développement des nouveau-nés proportionnellement à la dose . L'utilisation de SOLIFÉNACINE 5 mg doit être évitée pendant l'allaitement.
Interactions avec d'autres médicaments
Interactions pharmacologiques
L'utilisation concomitante d'autres médicaments ayant des propriétés anticholinergiques peut accentuer les effets thérapeutiques et les effets indésirables. Il faut respecter un intervalle d'environ une semaine après la fin du traitement par solifénacine avant d'entreprendre un autre traitement anticholinergique. L'effet thérapeutique de la solifénacine peut être atténué par l'administration concomitante d'agonistes des récepteurs cholinergiques.
La solifénacine peut réduire l'effet des médicaments qui stimulent la motilité gastro-intestinale, tels que le métoclopramide et le cisapride.
Interactions pharmacocinétiques
Des études menées in vitro ont montré qu'aux concentrations thérapeutiques la solifénacine n'inhibe pas les iso-enzymes CYP1A1/2, 2C9, 2C19, 2D6 ou 3A4 provenant de microsomes de foie humain. Il est donc peu probable que la solifénacine modifie la clairance des médicaments métabolisés par ces iso-enzymes du CYP.
Effet d'autres médicaments sur la pharmacocinétique de la solifénacine
La solifénacine est métabolisée par l'iso-enzyme CYP3A4. L'administration concomitante de 200 mg/jour ou de 400 mg/jour de kétoconazole, un puissant inhibiteur de cet iso-enzyme, s'est traduite respectivement par un doublement ou un triplement de l'ASC de la solifénacine. La dose maximale de solifénacine doit donc être limitée à 5 mg (5 ml) par jour chez les adultes ou à la dose initiale chez les enfants et les adolescents en cas d'administration concomitante de kétoconazole ou de doses thérapeutiques d'autres puissants inhibiteurs de l'iso-enzyme CYP3A4, par exemple le ritonavir, le nelfinavir, l'itraconazole .
L'administration concomitante de solifénacine et d'un puissant inhibiteur de l'iso-enzyme CYP3A4 est contre-indiquée chez les patients présentant une insuffisance rénale sévère ou une insuffisance hépatique modérée.
Les effets d'une induction enzymatique sur les paramètres pharmacocinétiques de la solifénacine et de ses métabolites n'ont pas été étudiés. De même, l'effet de substrats à plus forte affinité pour le CYP3A4 sur l'exposition à la solifénacine n'a pas fait l'objet d'étude.
Comme la solifénacine est métabolisée par l'iso-enzyme CYP3A4, des interactions pharmacocinétiques sont possibles avec d'autres substrats dotés d'une affinité plus élevée pour cet iso-enzyme (par exemple le vérapamil, le diltiazem) et avec des inducteurs de celui-ci (par exemple la rifampicine, la phénytoïne, la carbamazépine).
Effet de la solifénacine sur la pharmacocinétique d'autres médicaments
Contraceptifs oraux
Après la prise de solifénacine, aucune interaction pharmacocinétique entre la solifénacine et des contraceptifs oraux contenant une association d'éthinylestradiol et de lévonorgestrel n'a été observée.
Warfarine
La prise de solifénacine n'a pas modifié la pharmacocinétique de la R-warfarine ou de la S-warfarine et n'a pas eu d'incidence sur leur effet sur le temps de Quick.
Digoxine
Aucun effet sur la pharmacocinétique de la digoxine n'a été observé après la prise de solifénacine.

 Français
Français Русский
Русский