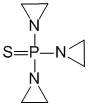Le
thiotépa est un agent alkylant, cytostatique, antinéoplasique, proche des moutardes azotées qui provoque des lésions de l'ADN.
Ses métabolites, particulièrement le TEPA, métabolite principal, ont des propriétés alkylantes.
La synthèse des désoxyribonucléoprotéines, indispensables à la mitose, est inhibée.
Pharmacocinétique - THIOTÉPA - usage parentéral
Après administration intraveineuse, le profil de la courbe de concentration plasmatique est biphasique.
Le produit est également distribué dans tout l'organisme.
Le thiotépa franchit la barrière hémato-méningée.
Après injection intracavitaire ou intratumorale, une certaine quantité de produit est retrouvée dans la circulation générale.
Après administration parentérale, le thiotépa se lie faiblement aux protéines plasmatiques.
Il est métabolisé probablement par les enzymes hépatiques principalement en TEPA et en d'autres composés alkylants cytotoxiques.
La demi-vie d'élimination est de 2 à 3 heures.
L'élimination est rénale.
Dosage - THIOTÉPA - usage parentéral
Lyophilisat pour usage parentéral
La solution doit être préparée extemporanément.
Voies IV et IM :
La dose habituelle est en général comprise entre 8 et 12 mg/m² par jour et par injection.
La dose totale pour une cure varie de 15 à 50 mg selon les protocoles.
Il est recommandé d'observer une période de repos de 4 à 6 semaines entre deux cures successives.
Voies intracavitaire (intrapleurale, intrapéricardiaque, intrapéritonéale) :
10 à 30 mg par injection. Etant donné les risques toxiques de résorption séreuse, ce mode d'administration exige une extrême prudence dans la posologie.
Instillations vésicales :
30 à 40 mg par instillation dilués dans 30 à 60 ml d'eau pour préparations injectables. La solution doit rester 1 à 2 heures dans la vessie.
Les intervalles entre les instillations sont variables selon les protocoles, entre 1 et 4 semaines.
Les posologies sont à ajuster selon la tolérance hématologique de l'instillation précédente.
Quelle que soit la voie d'administration, l'intervalle entre les cures dépend de la récupération hématologique.
Mode d'administration :
En cas d'extravasion, l'administration sera interrompue immédiatement.
Mode de manipulation :
La préparation des solutions injectables de cytotoxiques doit être obligatoirement réalisée par un personnel spécialisé et entraîné ayant une connaissance des médicaments utilisés, dans des conditions assurant la protection de l'environnement et surtout la protection du personnel qui manipule. Elle nécessite un local de préparation réservé à cet usage. Il est interdit de fumer, de manger, de boire dans ce local. Les manipulateurs doivent disposer d'un ensemble de matériel approprié à la manipulation notamment blouses à manches longues, masques de protection, calot, lunettes de protection, gants à usage unique stériles, champs de protection du plan de travail, conteneurs et sacs de collecte des déchets. Les excreta et les vomissures doivent être manipulés avec précaution. Les femmes enceintes doivent être averties et éviter la manipulation des cytotoxiques. Tout contenant cassé doit être traité avec les mêmes précautions et considéré comme un déchet contaminé. L'élimination des déchets contaminés se fait par incinération dans des conteneurs rigides étiquetés à cet effet.
Ces dispositions peuvent être envisagées dans le cadre du réseau de cancérologie (circulaire DGS/DH/98 N°98/188 du 24 mars 1998) en collaboration avec toute structure adaptée et remplissant les conditions requises.
Indications
Indications - THIOTÉPA - usage systémique
Cancer de l'ovaire.
Cancer du sein.
Cancer de la vessie (en instillation vésicale).
Contre-indications
Effets indésirables
Effets indésirables - THIOTÉPA - usage systémique
Hématologiques
Granulopénie, thrombopénie.
Non hématologiques
Digestifs : nausées et vomissements.
Vertiges, céphalées.
Aménorrhée, azoospermie.
Rares réactions allergiques.
Des cystites peuvent survenir en cas d'instillation vésicale.
Douleur au point d'injection.
Surdosage
L'apparition d'une chute importante des granulocytes ou des thrombocytes doit conduire à l'hospitalisation du patient en milieu spécialisé.
Grossesse/Allaitement
Le
thiotépa est contre-indiqué en cas de grossesse ou d'allaitement.
Interactions avec d'autres médicaments
Interactions communes à tous les cytotoxiques
En raison de l'augmentation du risque thrombotique lors des affectations tumorales, le recours à un traitement anticoagulant est fréquent. La grande variabilité de la coagulabilité au cours de ces affections, à laquelle s'ajoute l'éventualité d'une interaction entre les anticoagulants oraux et la chimiothérapie anticancéreuse, imposent, s'il est décidé de traiter le patient par anticoagulants oraux, d'augmenter la fréquence des contrôles de l'INR.
+ Vaccin antiamarile (fièvre jaune).
Risque de maladie vaccinale généralisée mortelle.
+ Phénytoïne (et, par extrapolation, fosphénytoïne.
Risque de survenue de convulsions par diminution de l'absorption digestive de la seule phénytoïne par le cytotoxique, ou bien risque de majoration de la toxicité ou de perte d'efficacité du cytotoxique par augmentation de son métabolisme hépatique par la phénytoïne ou la fosphénytoïne.
+ Vaccins vivants atténués sauf antiamarile
Risque de maladie vaccinale généralisée éventuellement mortelle. Ce risque est majoré chez les sujets déjà immunodéprimés par la maladie sous-jacente. Utiliser un vaccin inactivé lorsqu'il existe (poliomyélite).
Association à prendre en compte
+ Immunosuppresseurs
Immunodépression excessive avec risque de syndrome lymphoprolifératif.

 Français
Français Русский
Русский