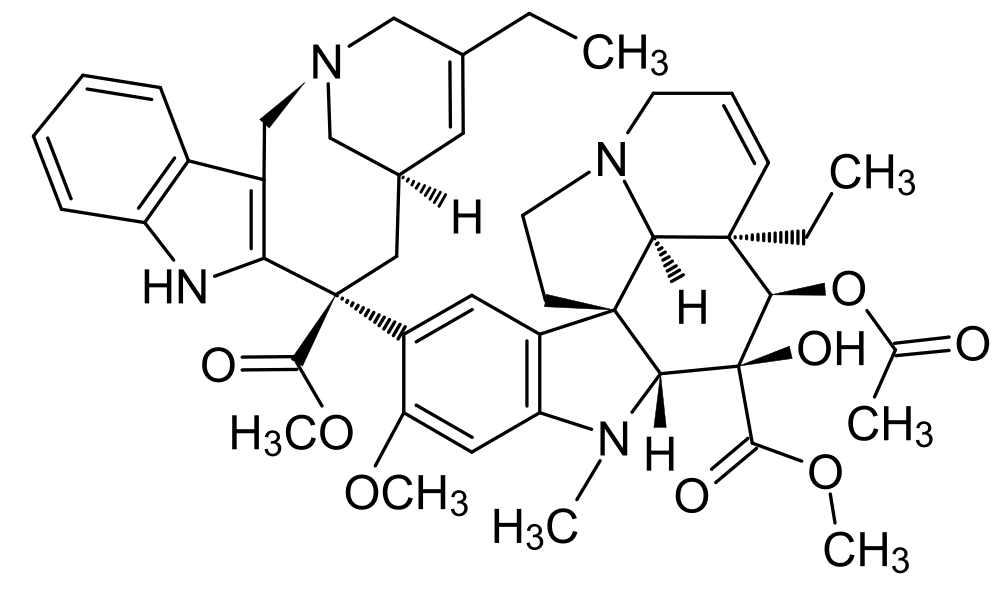
La vinorelbine est un antinéoplasique cytostatique de la famille des Vinca-Alcaloïdes mais à la différence des autres vinca-alcaloïdes, la partie catharantine de vinorelbine a été structurellement modifiée. Au niveau moléculaire, la vinorelbine agit sur l'équilibre dynamique de la tubuline au sein de l'appareil microtubulaire de la cellule. La vinorelbine inhibe la polymérisation de la tubuline. Elle agit préférentiellement sur les microtubules mitotiques, et n'affecte les microtubules axonaux qu'à forte concentration. Son pouvoir spiralisant de la tubuline est inférieur à celui de la vincristine.
La vinorelbine bloque la mitose en phase G2+M et provoque la mort cellulaire en interphase ou à la mitose suivante.
La sécurité et l'efficacité de la vinorelbine dans la population pédiatrique n'ont pas été établies.
Des données cliniques issues de deux études de phase II, non contrôlées (simple bras) utilisant la vinorelbine injectable chez 33 et 46 patients pédiatriques atteint de tumeurs solides récurrentes incluant des rhabdomyosarcomes, des sarcomes des tissus mous, des sarcomes d'Ewing, des liposarcomes, des sarcomes synoviaux, des fibrosarcomes, des cancers du système nerveux central, des ostéosarcomes, et des neuroblastomes, à des doses de 30 ou 33,75mg/m² jour 1 et 8 toutes les 3 semaines, ou 1 fois par semaine pendant 6 semaines toutes les 8 semaines n'a pas démontré d'efficacité clinique significative. Le profil de toxicité était similaire à celui reporté pour les patients adultes .
Pharmacocinétique - VINORELBINE - voie orale
Les paramètres pharmacocinétiques de la vinorelbine ont été évalués dans le sang.
Distribution
Le volume de distribution à l'état d'équilibre est grand : 21,2 l/kg (extrêmes : 7,5-39,7 l/kg) caractéristique d'une large distribution tissulaire.
Le taux de liaison aux protéines plasmatiques est faible (13,5 %). La vinorelbine est fortement liée aux cellules sanguines, en particulier aux plaquettes (78 %).
La pénétration de la vinorelbine dans les tissus pulmonaires est importante, comme en témoigne le rapport moyen des concentrations tissu/sérum, détecté par biopsie chirurgicale pulmonaire qui est supérieur à 300. La vinorelbine n'a pas été détectée au niveau du système nerveux central.
Biotransformation
Tous les métabolites de la vinorelbine sont formés par l'isoforme CYP3A4 des cytochromes P450 à l'exception de la 4-O-déacétyl-vinorelbine qui semble être formée par les carboxylestérases. La 4-O-déacétyl-vinorelbine est le seul métabolite actif et le principal métabolite détecté dans le sang. Le métabolisme de la vinorelbine ne fait intervenir ni glucuroconjugaison, ni sulfoconjugaison.
Élimination
La demi-vie moyenne d'élimination de la vinorelbine est d'environ 40 heures. La clairance totale est élevée : 0,72 l.h-1.kg-1 (extrêmes : 0,32-1,26 l. h-1.kg-1) et proche du débit sanguin hépatique. L'élimination rénale est faible (< 20% de la dose administrée) et se fait essentiellement sous forme inchangée. L'excrétion biliaire est la voie d'élimination prédominante, sous forme de vinorelbine inchangée qui est le composé majoritaire retrouvé et de ses métabolites.
Populations particulières
Insuffisants rénaux et hépatiques
Bien que l'impact des dysfonctions rénales sur l'élimination de la vinorelbine n'ait pas été évalué, il n'y a pas lieu de réduire la posologie chez les patients insuffisants rénaux car l'élimination rénale de vinorelbine est faible.
L'effet de l'insuffisance hépatique sur la pharmacocinétique de la vinorelbine a tout d'abord été étudié chez des patients atteints de métastases hépatiques consécutives à un cancer du sein. L'étude concluait qu'une modification de la clairance était observée uniquement lorsque le taux d'envahissement hépatique était supérieur à 75 %. Par ailleurs, une étude de phase I a été menée chez des patients à fonction hépatique altérée : 6 patients en insuffisance modérée (bilirubinémie ≤ 2 fois la LSN et taux de transaminases ≤ 5 fois la LSN) traités à la dose maximale de 25 mg/m2 et 8 patients en insuffisance sévère (bilirubinémie > 2 fois la LSN et/ou taux de transaminases > 5 fois la LSN) traités à la dose maximale de 20 mg/m2. La clairance totale chez ces patients était similaire à celle des patients à fonction hépatique normale et démontrait que la pharmacocinétique de la vinorelbine n'est pas modifiée en cas d'insuffisance hépatique quel qu'en soit le degré. Cependant, par mesure de précaution, il est recommandé de réduire la posologie à 20mg/m² et de surveiller étroitement les paramètres hématologiques chez les patients souffrant d'insuffisance hépatique sévère.
Personnes âgées
Une étude effectuée avec vinorelbine chez des personnes âgées (≥ 70 ans) souffrant d'un cancer du poumon non à petites cellules a démontré que les paramètres pharmacocinétiques de la vinorelbine n'étaient pas modifiés avec l'âge. Cependant, sachant que les personnes âgées sont fragiles, il est nécessaire d'être prudent lors de l'augmentation des doses de vinorelbine .
Relations pharmacocinétique/pharmacodynamique
Une forte corrélation a été établie entre l'exposition sanguine à la vinorelbine et la leucopénie ainsi que la neutropénie.
Dosage - VINORELBINE - voie orale
Capsule molle
En monothérapie :
Le schéma d'administration recommandé est le suivant :
Trois premières administrations :
Dose de 60 mg/m2 de surface corporelle, administrée une fois par semaine.
Administrations suivantes :
Au-delà de la troisième administration, il est recommandé d'augmenter la dose de VINORELBINE capsule molle à 80mg/m2 une fois par semaine, à l'exception des patients dont le nombre de neutrophiles a chuté une fois au-dessous de 500/mm3 ou plus d'une fois entre 500 et 1000/mm3 au cours des trois premières administrations réalisées à la dose de 60 mg/m2.
Nombre de | Neutrophiles | Neutrophiles | Neutrophiles | Neutrophiles |
neutrophiles lors des 3 | > 1000 | > 500 et< 1000 | > 500 et< 1000 | < 500 |
premières administrations |
| (1 épisode) | (2 épisodes) |
|
A 60mg/m²/semaine |
|
|
|
|
Dose recommandée à partir de la 4ème administration | 80 | 80 | 60 | 60 |
Modification de dose
Pour toute administration prévue à la dose de 80mg/m2, si le nombre de neutrophiles est inférieur à 500/mm3 ou s'il est plus d'une fois compris entre 500 et 1000/ mm3, il convient de retarder l'administration jusqu'à la normalisation de ce paramètre et de réduire la dose de 80 à 60 mg/m2 par semaine pour les 3 administrations suivantes.
Nombre de neutrophiles | Neutrophiles | Neutrophiles | Neutrophiles | Neutrophiles |
AU DELA DE LA 4eme | > 1000 | > 500 et < 1000 | > 500 et < 1000 | < 500 |
ADMINISTRATION A |
| (1 épisode) | (2 épisodes) |
|
80mg/m²/Semaine |
|
|
|
|
Dose recommandée lors de l'administration suivante | 80 | 60 |
Il est possible d'augmenter à nouveau la dose de 60 à 80mg/m² par semaine si le nombre de neutrophiles n'est pas inférieur à 500/mm3 ou plus d'une fois compris entre 500 et 1000/mm3 au cours des trois dernières administrations réalisées à 60mg/m², en accord avec le mode d'administration décrit pour les trois premières administrations.
En polychimiothérapie, la dose et le schéma thérapeutique seront adaptés selon le protocole de traitement
Les résultats des essais cliniques démontrent qu'une dose per os de 80 mg/m2 correspond à une dose IV de 30 mg/m2 et qu'une dose per os de 60 mg/m2 correspond à une dose IV de 25 mg/m2.
Ceci a été la base des protocoles d'association alternant forme IV et orale améliorant le confort du patient.
Pour les protocoles d'association, la dose et le schéma thérapeutique seront adaptés selon le protocole de traitement.
Même pour les patients dont la SC > 2 m2, la dose totale ne doit jamais dépasser 120 mg par semaine (posologie à 60 mg/ m2) ou 160 mg par semaine (posologie à 80 mg/ m2).
Mode d'administration
VINORELBINE doit être administré uniquement par voir orale.
VINORELBINE capsule molle doit être avalée avec de l'eau sans mâcher ni sucer la capsule.
II est recommandé de prendre la capsule à la fin d'un repas.
Administration chez les personnes âgées :
L'expérience clinique n'a pas permis d'identifier des différences significatives parmi les personnes âgées au regard du taux de réponse bien qu'une sensibilité plus importante chez certains de ces patients ne peut être exclue. L'âge ne modifie pas la pharmacocinétique de la vinorelbine.
Administration chez les enfants :
La tolérance et l'efficacité chez les enfants n'ont pas été étudiées, par conséquent, l'administration de VINORELBINE est déconseillée .
Administration chez les patients souffrant d'insuffisance hépatique :
VINORELBINE peut être administré à la dose standard de 60mg/m² par semaine chez les patients atteint d'insuffisance hépatique légère (bilirubine < 1.5 x LSN, et ALAT et/ou ASAT de 1,5 à 2,5 x LSN). Chez les patient atteints d'insuffisance hépatique modérée (bilirubine de 1,5 à 3 x LSN, quelque soit le niveau d'ALAT et d'ASAT), VINORELBINE doit être administré à une dose de 50mg/m²/semaine. L'administration de VINORELBINE chez l'insuffisant hépatique sévère n'est pas recommandée car il n'y a pas de données suffisantes pour déterminer la pharmacocinétique, l'efficacité et la sécurité de VINORELBINE dans cette population
Administration chez les patients souffrant insuffisance rénale :
L'excrétion rénale étant faible, il n'y a pas de justification pharmacocinétique pour réduire la dose de VINORELBINE chez des patients insuffisants rénaux .
Instructions pour l'utilisation et la manipulation de VINORELBINE orale .
Dosage - VINORELBINE - usage parentéral
Solution injectable
Voie intraveineuse stricte.
En monothérapie, la dose habituelle est de 25 à 30 mg/m2 administrée à fréquence hebdomadaire.
En polychimiothérapie, la dose et la fréquence sont fonction du protocole. La dose injectée doit être diluée dans un soluté physiologique ou glucosé à 5% (125 ml par exemple) et perfusée sur une courte période (6 à 10 minutes). L'administration devra être suivie d'un rinçage abondant de la veine par le soluté physiologique.
Insuffisance hépatique .
Insuffisance rénale .
La tolérance et l'efficacité de vinorelbine n'ont pas été étudiées chez l'enfant.
Attention: il est extrêmement important de s'assurer que l'aiguille est correctement introduite dans la voie d'abord avant de commencer l'injection. En cas d'extravasation, il peut survenir une cellulite voire une nécrose. Il convient alors d'interrompre immédiatement l'injection et d'aspirer le maximum de produit extravasé, la quantité restante doivent être administrée par une autre veine. L'application de chaleur modérée facilite la diffusion du produit et semble réduire le risque de cellulite. |
En cas de contact accidentel avec l'il, faire immédiatement un lavage abondant de l'il.
Modalités de manipulation
La préparation des solutions injectables de cytotoxiques doit être obligatoirement réalisée par un personnel spécialisé et entraîné ayant une connaissance des médicaments utilisés, dans des conditions assurant la protection de l'environnement et surtout la protection du personnel qui manipule. Elle nécessite un local de préparation réservé à cet usage. Il est interdit de fumer, de manger, de boire dans ce local. Les manipulateurs doivent disposer d'un ensemble de matériel approprié à la manipulation notamment blouses à manches longues, masques de protection, calot, lunettes de protection, gants à usage unique stériles, champs de protection du plan de travail, conteneurs et sacs de collecte des déchets. Les excréta et les vomissures doivent être manipulés avec précaution. Les femmes enceintes doivent être averties et éviter la manipulation des cytotoxiques. Tout contenant cassé doit être traité avec les mêmes précautions et considéré comme un déchet contaminé. L'élimination des déchets contaminés se fait par incinération dans des conteneurs rigides étiquetés à cet effet. |
Ces dispositions peuvent être envisagées dans le cadre du réseau de cancérologie (circulaire DGS/DH/98 N°98/188 du 24 mars 1998) en collaboration avec toute structure adaptée et remplissant les conditions requises.
Solution à diluer pour perfusion
Voie intraveineuse stricte.
En monothérapie, la dose habituelle est de 25 à 30 mg/m2 administrée à fréquence hebdomadaire.
En polychimiothérapie, la dose et la fréquence sont fonction du protocole. La dose injectée doit être diluée dans un soluté physiologique (125 ml par exemple) et perfusée sur une courte période (6 à 10 minutes). L'administration devra être suivie d'un rinçage abondant de la veine par le soluté physiologique.
Insuffisance hépatique .
Insuffisance rénale .
La tolérance et l'efficacité de vinorelbine n'ont pas été étudiées chez l'enfant.
Attention: il est extrêmement important de s'assurer que l'aiguille est correctement introduite dans la voie d'abord avant de commencer l'injection. En cas d'extravasation, il peut survenir une cellulite voire une nécrose. Il convient alors d'interrompre immédiatement l'injection et d'aspirer le maximum de produit extravasé, la quantité restante doivent être administrée par une autre veine. L'application de chaleur modérée facilite la diffusion du produit et semble réduire le risque de cellulite. |
En cas de contact accidentel avec l'il, faire immédiatement un lavage abondant de l'il.
Modalités de manipulation
La préparation des solutions injectables de cytotoxiques doit être obligatoirement réalisée par un personnel spécialisé et entraîné ayant une connaissance des médicaments utilisés, dans des conditions assurant la protection de l'environnement et surtout la protection du personnel qui manipule. Elle nécessite un local de préparation réservé à cet usage. Il est interdit de fumer, de manger, de boire dans ce local. Les manipulateurs doivent disposer d'un ensemble de matériel approprié à la manipulation notamment blouses à manches longues, masques de protection, calot, lunettes de protection, gants à usage unique stériles, champs de protection du plan de travail, conteneurs et sacs de collecte des déchets. Les excréta et les vomissures doivent être manipulés avec précaution. Les femmes enceintes doivent être averties et éviter la manipulation des cytotoxiques. Tout contenant cassé doit être traité avec les mêmes précautions et considéré comme un déchet contaminé. L'élimination des déchets contaminés se fait par incinération dans des conteneurs rigides étiquetés à cet effet. |
Ces dispositions peuvent être envisagées dans le cadre du réseau de cancérologie (circulaire DGS/DH/98 N°98/188 du 24 mars 1998) en collaboration avec toute structure adaptée et remplissant les conditions requises.
Indications
Indications - VINORELBINE - usage systémique
cancer du poumon non à petites cellules,
cancer du sein métastatique.
Contre-indications
Ce médicament est contre-indiqué dans les cas suivants :
Hypersensibilité connue à la vinorelbine ou à d'autres vinca-alcaloïdes, ou à tout autre constituant de la Navelbine.
Taux de neutrophiles inférieur à 1500/mm3 ou infection sévère actuelle ou récente (dans les 2 semaines).
Taux de plaquettes < 100000/mm3.
Allaitement .
En association avec le vaccin contre la fièvre jaune

 Français
Français Русский
Русский