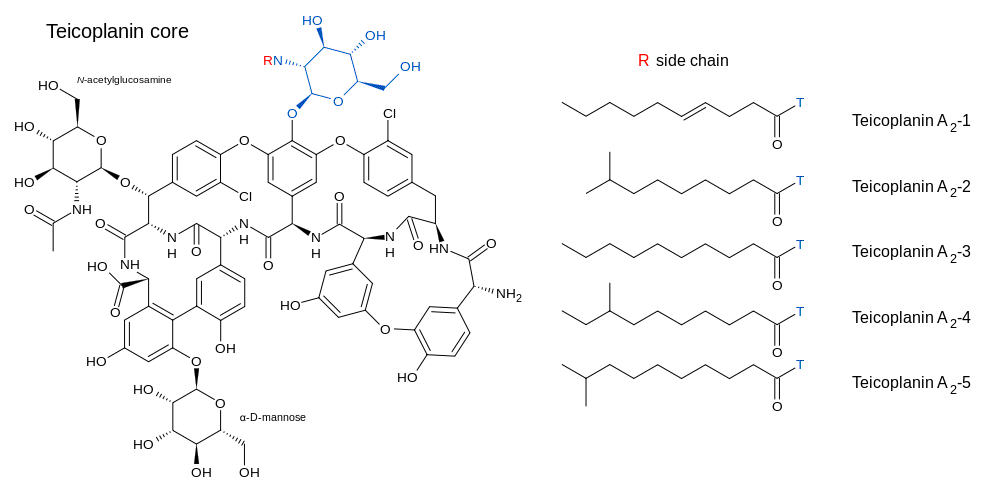
La teicoplanine inhibe la croissance des bactéries sensibles en interférant avec la synthèse de leur paroi cellulaire au niveau d'un site différent de celui qui est affecté par les bêta-lactamines. La synthèse du peptidoglycane est bloquée par une liaison spécifique à des résidus D-alanyl-D-alanine.
Mécanisme de résistance
Une résistance à la teicoplanine peut être basée sur les mécanismes suivants :
Modification de la structure cible : cette forme de résistance est particulièrement apparue chez Enterococcus faecium. La modification concerne le remplacement de la fonction de la chaine terminale d'acides aminés D-alanyl-D-alanine en un précurseur de muréine D-Ala-D-lactate, ce qui réduit l'affinité pour la vancomycine. Les enzymes responsables sont une D-lactate déshydrogénase ou ligase nouvellement synthétisées.
La réduction de la sensibilité ou la résistance des staphylocoques à la teicoplanine repose sur la surproduction des précurseurs de muréine auxquels la teicoplanine se lie.
Une résistance croisée entre la teicoplanine et la vancomycine peut apparaître. Certains entérocoques résistants à la vancomycine sont sensibles à la teicoplanine (phénotype Van-B).
Concentrations critiques
Les valeurs seuils des CMI selon l'EUCAST (European Committee on Antimicrobial Susceptibility Testing), version 7.1, 10 Mars 2017, sont présentées dans le tableau suivant :
Microorganismes | Sensible | Résistant |
Staphylococcus aureus a,b | ≤ 2 mg/L | > 2 mg/L |
Staphylocoques à coagulase-negative a, b | ≤ 4 mg/L | > 4 mg/L |
Enterococcus spp. | ≤ 2 mg/L | > 2 mg/L |
Streptococcus groupes A, B, C, G b | ≤ 2 mg/L | > 2 mg/L |
Streptococcus pneumoniae b | ≤ 2 mg/L | > 2 mg/L |
Streptocoques du groupe viridans b | ≤ 2 mg/L | > 2 mg/L |
Anaérobies à Gram positif sauf Clostridium difficile Seuils PK/PD (non liés à l'espèce) | DI DI | DI DI |
a. Les CMI des glycopeptides dépendent de la méthode et elles doivent être déterminées par microdilution en bouillon (référence ISO 20776). Les souches de S. aureus ayant une CMI pour la vancomycine de 2 mg/L sont à la limite de la distribution des CMI pour les souches de phénotype sauvage ce qui peut aboutir à une réponse clinique altérée. Le seuil de résistance pour S. aureus a été abaissé à 2 mg/L afin d'éviter le classement de souches GISA en intermédiaires, car les infections graves dues aux souches GISA ne peuvent être traitées par des doses accrues de vancomycine ou de teicoplanine.
b. La proportion d'isolats résistants est rare ou non encore signalée. Les résultats des tests d'identification de sensibilité antimicrobienne de ces isolats doivent être confirmés, et l'isolat doit être adressé à un laboratoire de référence. DI indique que les données sont insuffisantes pour montrer que les organismes ou les groupes d'organismes en question sont une cible adéquate pour le traitement par le médicament.
Une CMI avec un commentaire, mais sans classement S, I ou R associé, peut être signalée.
Relation pharmacocinétique/pharmacodynamique
L'activité antibactérienne de la teicoplanine dépend essentiellement de la durée pendant laquelle la concentration de cette substance est plus élevée que sa concentration minimale inhibitrice (CMI) sur l'agent pathogène.
Sensibilité
La prévalence de la résistance peut varier en fonction de la géographie et du temps pour certaines espèces, et il est donc utile de disposer d'informations sur la prévalence de la résistance locale, surtout pour le traitement d'infections sévères. Si nécessaire, il est souhaitable d'obtenir un avis spécialisé principalement lorsque l'intérêt du médicament dans certaines infections peut être mis en cause du fait du niveau de prévalence de la résistance locale.
Espèces habituellement sensibles Bactéries aérobies à Gram positif Corynebacterium jeikeium a Enterococcus faecalis Staphylococcus aureus (dont souches résistantes à la méticilline) Streptococcus agalactiae Streptococcus dysgalactiae subsp. equisimilis a (streptocoques des groupes C & G) Streptococcus pneumoniae Streptococcus pyogenes Streptocoques du groupe viridans a b Bactéries anaérobies à Gram positif Clostridium difficile a Peptostreptococcus spp.a |
Espèces inconstamment sensibles (Résistance acquise > 10 %) Bactéries aérobies à Gram positif Enterococcus faecium Staphylococcus epidermidis Staphylococcus haemolyticus Staphylococcus hominis |
Bactéries naturellement résistantes Toutes les bactéries à Gram négatif Autres bactéries Chlamydia spp. Chlamydophila spp. Legionella pneumophila Mycoplasma spp. |
a. Aucune donnée actuelle n'était disponible au moment de la publication des tableaux. Les principales données de la littérature, les documents de base et les recommandations thérapeutiques présument d'une sensibilité. b. Terme collectif pour un groupe hétérogène d'espèces streptococciques. Le taux de résistance peut varier selon l'espèce streptococcique en cause. |
Pharmacocinétique
Pharmacocinétique - TÉICOPLANINE - usage parentéral
Absorption
La teicoplanine est administrée par voie parentérale (intraveineuse ou intramusculaire). Après une administration intramusculaire, la biodisponibilité de la teicoplanine (comparativement à une administration intraveineuse) est quasi-totale (90 %). Après six administrations journalières intramusculaires de 200 mg, la concentration maximale moyenne (écart type) de teicoplanine (Cmax) est de 12,1 (0,9) mg/L et est obtenue 2 heures après administration.
Après une dose de charge de 6 mg/kg administrée par voie intraveineuse toutes les 12 heures pour 3 à 5 administrations, les valeurs de la Cmax sont comprises entre 60 et 70 mg/L et celles de la concentration résiduelle sont habituellement supérieures à 10 mg/L. Après une dose de charge intraveineuse de 12 mg/kg administrée toutes les 12 heures pour 3 administrations, les valeurs moyennes de la Cmax et de la concentration résiduelle sont respectivement estimées à environ 100 mg/L et 20 mg/L.
Après une dose d'entretien de 6 mg/kg administrée une fois par jour, les valeurs de la Cmax et de la concentration résiduelle sont respectivement d'environ 70 mg/L et 15 mg/L. Après une dose d'entretien de 12 mg /kg administrée une fois par jour, les concentrations résiduelles vont de 18 à 30 mg/L.
La teicoplanine administrée par voie orale n'est pas absorbée dans le tractus digestif. À la suite de l'administration par voie orale d'une dose unique de 250 ou 500 mg chez des sujets sains, la teicoplanine n'a pas été détectée dans le sérum ni dans l'urine, mais a été retrouvée uniquement dans les fèces (environ 45 % de la dose administrée) sous forme inchangée.
Distribution
La liaison aux protéines plasmatiques humaines varie de 87,6 à 90,8 % indépendamment des concentrations de teicoplanine. La teicoplanine est principalement liée à la sérum-albumine humaine. La teicoplanine ne diffuse pas dans les érythrocytes.
Le volume de distribution à l'état d'équilibre (Vss) varie de 0,7 à 1,4 L/kg. Les valeurs les plus élevées du Vss ont été observées lors d'études récentes, dans lesquelles la durée de la période de prélèvements était supérieure à 8 jours.
La teicoplanine diffuse principalement dans les poumons, le myocarde et les tissus osseux avec des rapports concentration tissulaire/concentration sérique supérieurs à 1. Ces rapports variaient de 0,5 à 1 dans le liquide de phlyctène, le liquide synovial et le liquide péritonéal. Le taux d'élimination de la teicoplanine du liquide péritonéal est identique à celui de son élimination du sérum. Dans le liquide pleural et les tissus adipeux sous-cutanés, les rapports concentration tissulaire/concentration sérique sont compris entre 0,2 et 0,5. La teicoplanine ne pénètre pas facilement dans le liquide céphalorachidien (LCR).
Biotransformation
La teicoplanine sous forme inchangée est le principal composé identifié dans le plasma et l'urine, ce qui indique qu'elle est peu métabolisée .Deux métabolites, formés probablement par hydroxylation, représentent 2 à 3 % de la dose administrée.
Élimination
La teicoplanine est principalement excrétée sous forme inchangée par voie urinaire (80 % en 16 jours), tandis que 2,7 % de la dose administrée sont récupérés dans les fèces (à la suite d'une excrétion biliaire) au cours des 8 jours suivant l'administration.
La demi-vie d'élimination de la teicoplanine a varié de 100 à 170 heures lors des études les plus récentes au cours desquelles la durée des périodes de prélèvements était d'environ 8 à 35 jours.
La clairance totale de la teicoplanine est faible, de 10 à 14 mL/h/kg, et sa clairance rénale est de 8 à 12 mL/h/kg, ce qui indique qu'elle est principalement excrétée par des mécanismes rénaux.
Linéarité
La pharmacocinétique de la teicoplanine est linéaire pour des doses de 2 à 25 mg/kg.
Populations particulières
Patients insuffisants rénaux :
La teicoplanine est éliminée par voie rénale, et son élimination diminue donc selon le degré d'insuffisance rénale. Les clairances totale et rénale de la teicoplanine dépendent de la clairance de la créatinine.
Patients âgés :
Les paramètres pharmacocinétiques de la teicoplanine ne sont pas modifiés chez les patients âgés, sauf en cas d'insuffisance rénale.
Population pédiatrique
Comparativement à l'adulte, la clairance totale est plus élevée chez l'enfant (15,8 mL/h/kg pour des nouveau-nés, 14,8 mL/h/kg pour un âge moyen de 8 ans) et la demi-vie d'élimination plus courte (40 heures pour les nouveau-nés ; 58 heures pour 8 ans).
Dosage
Dosage - TÉICOPLANINE - usage parentéral
Poudre et solvant pour solution injectable pour perfusion ou buvable
La dose et la durée du traitement doivent être adaptées selon le type et la sévérité de l'infection et la réponse clinique du patient, et selon des facteurs liés au patient tels que l'âge et la fonction rénale.
Mesure des concentrations sériques
Les concentrations sériques résiduelles de teicoplanine doivent être surveillées à l'état d'équilibre après administration de la dernière dose de charge afin de vérifier que la concentration sérique résiduelle minimale a été atteinte :
Pour la plupart des infections à Gram positif, cette concentration résiduelle de teicoplanine doit être d'au moins 10 mg/L (mesure par chromatographie liquide à haute performance [HPLC]), ou d'au moins 15 mg/L (mesure par méthode de dosage immunologique par polarisation de fluorescence [FPIA]).
Pour une endocardite ou autres infections sévères, cette concentration résiduelle de teicoplanine doit être de 15 à 30 mg/L (mesure par HPLC) ou de 30 à 40 mg/L (mesure par méthode FPIA).
Durant le traitement d'entretien, les concentrations sériques résiduelles de teicoplanine doivent être mesurées au moins une fois par semaine dans le but de vérifier le maintien de ces concentrations.
Patients adultes et patients âgés présentant une fonction rénale normale
Indications | Dose de charge | Dose d'entretien |
Dose de charge | Concentrations résiduelles ciblées pour les jours 3 à 5 | Dose d'entretien | Concentrations résiduelles ciblées durant le traitement d'entretien |
- Infections compliquées de la peau et des tissus mous | 6 mg/kg de poids corporel toutes les 12 heures pour 3 administrations par voie intraveineuse ou intramusculaire. | > 15 mg/L(1) | 6 mg/kg de poids corporel par voie intraveineuse ou intramusculaire une fois par jour | > 15 mg/L(1) Une fois par semaine |
- Pneumonies |
- Infections urinaires compliquées |
- Infections ostéoarticulaires | 12 mg/kg de poids corporel toutes les 12 heures pour 3 à 5 administrations par voie intraveineuse | > 20 mg/L(1) | 12 mg/kg de poids corporel par voie intraveineuse ou intramusculaire une fois par jour | > 20 mg/L(1) |
- Endocardite infectieuse | 12 mg/kg de poids corporel toutes les 12 heures pour 3 à 5 administrations par voie intraveineuse. | 30 à 40 mg/L(1) | 12 mg/kg de poids corporel par voie intraveineuse ou intramusculaire une fois par jour | > 30 mg/L(1) |
(1) Mesure par méthode FPIA
La posologie doit être adaptée au poids du patient.
Durée du traitement
La durée du traitement doit être décidée sur la base de la réponse clinique. Pour le traitement d'une endocardite infectieuse, une durée minimale de 21 jours est habituellement considérée appropriée. La durée du traitement ne doit pas excéder 4 mois.
Association d'antibiotiques
Le spectre d'activité antibactérienne de la teicoplanine est étroit (Gram positif). Dans certaines infections, un traitement par teicoplanine en monothérapie peut être envisagé uniquement si le germe est déjà identifié, et s'il est sensible ou s'il existe une forte probabilité qu'il le soit.
Diarrhée et colite associées à une infection à Clostridium difficile
La dose recommandée est de 100 - 200 mg par voie orale deux fois par jour pendant 7 à 14 jours.
Patients âgés
Aucune adaptation posologique n'est nécessaire, sauf en cas de fonction rénale altérée (voir ci-dessous).
Patients adultes et patients âgés présentant une altération de la fonction rénale
Aucune adaptation posologique n'est nécessaire jusqu'au quatrième jour de traitement, moment auquel la dose doit être adaptée pour maintenir une concentration sérique résiduelle d'au moins 10 mg/L lorsque la mesure est effectuée par HPLC, ou d'au moins 15 mg/L lorsqu'elle est mesurée par la méthode FPIA.
Après le quatrième jour de traitement :
En cas d'insuffisance rénale légère ou modérée (clairance de la créatinine de 30 à 80 mL/min) : la dose d'entretien doit être diminuée de moitié, soit par l'administration de la dose un jour sur deux, soit par l'administration de la moitié de la dose une fois par jour.
En cas d'insuffisance rénale sévère (clairance de la créatinine inférieure à 30 mL/min) et chez les patients hémodialysés : la dose doit correspondre à un tiers de la dose habituelle, soit par l'administration de la dose unitaire initiale tous les trois jours, soit par l'administration d'un tiers de la dose une fois par jour.
La teicoplanine n'est pas éliminée par hémodialyse.
Patients sous dialyse péritonéale continue ambulatoire (DPCA)
Après une dose de charge intraveineuse unique de 6 mg/kg de poids corporel, 20 mg/L sont administrés dans chaque poche de solution de dialyse la première semaine, 20 mg/L dans une poche sur deux la seconde semaine, puis 20 mg/L dans la poche de nuit la troisième semaine.
Population pédiatrique
Chez les enfants de plus de 12 ans, les recommandations posologiques sont les mêmes que chez les adultes.
Nouveau-nés et nourrissons jusqu'à l'âge de 2 mois :
Dose de charge
Une dose unique de 16 mg/kg de poids corporel administrée par perfusion intraveineuse le premier jour.
Dose d'entretien
Une dose de 8 mg/kg de poids corporel administrée par perfusion intraveineuse une fois par jour.
Enfants (2 mois à 12 ans) :
Dose de charge
Une dose de 10 mg/kg de poids corporel administrée par voie intraveineuse toutes les 12 heures, répétée 3 fois.
Dose d'entretien
Une dose de 6 à 10 mg/kg de poids corporel administrée par voie intraveineuse une fois par jour.
Mode d'administration
La teicoplanine peut être administrée par voie intraveineuse ou intramusculaire. L'injection intraveineuse peut être administrée en bolus en 3 à 5 minutes ou par perfusion sur 30 minutes.
Seule la perfusion peut être utilisée chez les nouveau-nés.
La voie orale est recommandée pour le traitement des diarrhées et des colites associées à Clostridium Difficile.
Indications
Indications - TÉICOPLANINE - usage systémique
TÉICOPLANINE est indiqué chez les adultes et les enfants dès la naissance pour le traitement parentéral des infections suivantes :
Infections compliquées de la peau et des tissus mous,
Infections ostéoarticulaires,
Pneumonies nosocomiales,
Pneumonies communautaires,
Infections urinaires compliquées,
Endocardite infectieuse,
Péritonite associée à une dialyse péritonéale continue ambulatoire (DPCA),
Bactériémie survenant en association à l'une des indications mentionnées ci-dessus.
TÉICOPLANINE est également indiqué comme alternative thérapeutique orale dans le traitement des diarrhées et colites associées à une infection à Clostridium difficile.
Dans certains cas, la teicoplanine doit être administrée en association à d'autres antibactériens.
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens.
Effets indésirables
Effets indésirables - TÉICOPLANINE - usage systémique
Tableau listant les effets indésirables
Tous les effets indésirables survenus avec une incidence plus élevée que sous placebo et chez plus d'un patient sont mentionnés dans le tableau ci-dessous en utilisant la convention suivante :
Très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Au sein de chaque groupe de fréquence, les effets indésirables sont présentés par ordre de gravité décroissante.
Des effets indésirables doivent être recherchés plus particulièrement quand la teicoplanine est administrée à des doses de 12 mg/kg de poids corporel deux fois par jour .
Classe de systèmes d'organes | Fréquent (≥ 1/100 à < 1/10) | Peu fréquent (≥ 1/1 000 à < 1/100) | Rare (≥ 1/10 000 à < 1/1 000) | Très rare (< 1/10 000) | Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) |
Infections et infestations | | | Abcès | | Surinfection (prolifération de micro-organismes non sensibles) |
Affections hématolo-giques et du système lymphatique | | Leucopénie, thrombopénie, éosinophilie | | | Agranulocytose, neutropénie |
Affections du système immunitaire | | Réaction anaphylactique (anaphylaxie) | | | Syndrome d'hypersensibilité médicamenteuse avec hyperéosinophilie et symptômes systémiques (DRESS) Choc anaphylactique |
Affections du système nerveux | | Sensations vertigineuses, céphalées | | | Convulsions |
Affections de l'oreille et du labyrinthe | | Surdité, perte d'audition , acouphènes, troubles vestibulaires | | | |
Affections vasculaires | | Phlébite | | | Thrombophlébite |
Affections respiratoires, thoraciques et médiastinales | | Bronchospasme | | | |
Affections gastro-intestinales | | Diarrhée, vomissements, nausées | | | |
Affections de la peau et du tissu sous-cutané | Éruption, érythème, prurit | | Red man syndrome (par ex. rougeur de la partie supérieure du corps) . | | Nécrolyse épidermique toxique, Syndrome de Stevens-Johnson, érythème polymorphe, angidème (dème de Quincke), dermatite exfoliatrice, urticaire |
Affections du rein et des voies urinaires | | Augmentation de la créatininémie | | | Insuffisance rénale (y compris insuffisance rénale aiguë) |
Troubles généraux et anomalies au site d'administra-tion | Douleur, pyrexie | | | | Abcès au site d'injection, frissons |
Investigations | | Augmentation des transaminases (anomalie transitoire des transaminases), augmentation du taux sérique de phosphatase alcaline (anomalie transitoire des phosphatases alcalines), augmentation de la créatininémie (élévation transitoire de la créatininémie) | | | |
Surdosage
Symptômes
Des cas d'administration accidentelle de doses excessives à des patients pédiatriques ont été rapportés. Dans un cas, une agitation est apparue chez un nouveau-né âgé de 29 jours qui avait reçu 400 mg par voie intraveineuse (95 mg/kg).
Prise en charge
Le traitement d'un surdosage de teicoplanine doit être symptomatique.
La teicoplanine n'est pas éliminée par hémodialyse et ne l'est que lentement par dialyse péritonéale.
Grossesse/Allaitement
Grossesse
Il existe des données limitées sur l'utilisation de la teicoplanine chez la femme enceinte. Les études effectuées chez l'animal ont mis en évidence une toxicité sur la reproduction à fortes doses : une augmentation de la mortinatalité et de la mortalité néonatale a été observée chez le rat. Le risque potentiel pour l'Homme est inconnu.
La teicoplanine ne doit donc pas être utilisée au cours de la grossesse sauf en cas de nécessité absolue. Un risque potentiel de lésions de l'oreille interne et de lésions rénales chez le ftus ne peut être exclu .
Allaitement
On ne sait pas si la teicoplanine est excrétée dans le lait maternel. Il n'existe pas de données suffisantes sur l'excrétion de la teicoplanine dans le lait animal. La décision de continuer/interrompre l'allaitement ou de continuer/interrompre le traitement par teicoplanine doit être prise en prenant en compte le bénéfice de l'allaitement pour l'enfant au regard du bénéfice du traitement pour la femme.
Fertilité
Les études sur la reproduction chez l'animal n'ont pas montré de signe d'altération de la fertilité.
Interactions avec d'autres médicaments
Aucune étude spécifique d'interaction n'a été réalisée.
Les solutions de teicoplanine et d'aminosides sont incompatibles et ne doivent pas être mélangées lors d'administration parentérale ; cependant, elles sont compatibles avec le liquide de dialyse de la DPCA et peuvent être librement utilisées dans le traitement d'une péritonite associée à une DPCA.
La teicoplanine doit être utilisée avec prudence en association ou séquentiellement avec d'autres médicaments présentant un potentiel néphrotoxique ou ototoxique connu. Parmi ces médicaments figurent aminosides, colistine, amphotéricine B, ciclosporine, cisplatine, furosémide et acide étacrynique . Il n'existe cependant aucune preuve d'une toxicité synergique en association avec la teicoplanine.
Lors d'études cliniques, la teicoplanine a été administrée à de nombreux patients recevant déjà divers médicaments, y compris d'autres antibiotiques, des antihypertenseurs, des anesthésiques, des médicaments à visée cardiaque et des antidiabétiques, sans signe d'interaction défavorable.
Population pédiatrique
Les études d'interactions n'ont été menées que chez l'adulte.

 Français
Français Русский
Русский