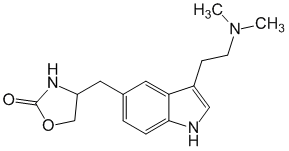
Pharmacodynamique
(N: système nerveux central).
Lors des études précliniques, le
zolmitriptan s'est avéré être un agoniste sélectif des récepteurs recombinant humains vasculaires 5HT
1Dα et 5HT
1Dβ. Le zolmitriptan présente une forte affinité pour les récepteurs 5HT1D et une faible affinité pour les récepteurs 5HT1A. Le zolmitriptan ne présente aucune affinité (mesurée par des dosages de radio ligands) ni effets pharmacologiques significatifs sur les récepteurs sérotoninergiques 5HT
2,5HT
3, 5HT
4, adrénergiques alpha1, alpha
2, beta
1, histaminiques H
1, H
2, muscariniques, dopaminergiques 1 ou 2.
Le système trigémino-vasculaire est impliqué dans la physiopathologie de la migraine.
Chez l'animal, le zolmitriptan, grâce à son activité agoniste sur les récepteurs 5HT1, induit une vasoconstriction et une inhibition de la libération du peptide lié au gène de la calcitonine (CGRP), du peptide vasoactif intestinal (VIP) et de la substance P. Ces deux effets (vasoconstriction et inhibition de la libération de neuropeptides) sont vraisemblablement à l'origine de l'amélioration des crises de migraine, représentée par une disparition de la douleur et des autres symptômes de la migraine dans l'heure suivant l'administration.
Le zolmitriptan est efficace dans le traitement de la phase céphalalgique de la crise de migraine cataméniale.
Outre ses actions périphériques, le zolmitriptan traverse la barrière hémato-méningée et peut accéder ainsi non seulement aux centres périphériques de la migraine mais aussi à ceux du tronc cérébral. Il bloque la voie réflexe vasodilatatrice utilisant les fibres orthodromiques du trijumeau et l'innervation parasympathique de la circulation cérébrale et inhibe ainsi la libération du VIP qui en est le principal neurotransmetteur.
Un essai clinique réalisé chez 696 adolescents migraineux n'a pas montré de supériorité du zolmitriptan en comprimés dosés à 2,5 mg, 5 mg et 10 mg, par rapport au placebo. L'efficacité n'a pas été démontrée.
Pharmacocinétique
Pharmacocinétique - ZOLMITRIPTAN - voie orale
Absorption
Après administration orale, le zolmitriptan est rapidement absorbé chez l'homme (absorption ≥ 64 %) avec une biodisponibilité de l'ordre de 40 %.
Après une dose unique comprise entre 2,5 et 50 mg, 75 % de la Cmax sont atteints en moins d'une heure. Les concentrations plasmatiques sont ensuite maintenues pendant 4 à 6 heures.
L'absorption n'est pas modifiée par la nourriture.
La répétition des prises n'entraîne pas d'accumulation du produit.
Distribution
Après administration intraveineuse, le volume de distribution est de 2,4 l/kg. La fixation aux protéines plasmatiques est négligeable (25 %).
Métabolisme
Le zolmitriptan est métabolisé essentiellement au niveau hépatique. Les trois principaux métabolites sont: l'acide indole acétique (principal métabolite urinaire et plasmatique), les analogues N-oxyde et N-desméthyl du zolmitriptan. Ce dernier est le seul métabolite actif, agoniste sérotoninergique 5HT1D, 2 à 6 fois plus puissant que la molécule mère chez l'animal.
Les concentrations plasmatiques de ce métabolite représentent environ la moitié de celles du zolmitriptan; il participe vraisemblablement à l'activité thérapeutique du produit.
Elimination
Plus de 60 % de la dose administrée par voie orale sont retrouvés dans les urines (principalement sous forme d'acide indole acétique) et environ 30 % dans les fèces sous forme inchangée.
Après administration intraveineuse, la clairance plasmatique totale est de 10 ml/min/kg, dont le tiers est représenté par la clairance rénale.
Les demi-vies d'élimination du zolmitriptan et de ses métabolites sont approximativement de 2,5 à 3 heures.
Formes comprimé orodispersible
La bioéquivalence entre le comprimé orodispersible et le comprimé standard de zolmitriptan a été démontrée en terme d'AUC et de Cmax pour le zolmitriptan et son métabolite actif (C 183C91) N-déméthylé lors d'une étude de pharmacologie clinique.
Les valeurs Tmax du métabolite actif N-déméthylé du zolmitriptan sont comparables pour les deux formes: -comprimé orodispersible (1 - 6 heures, médiane 3 heures) et - comprimé standard (0,75 - 5 heures, médiane 3 heures). Le tmax de zolmitriptan peut être allongé pour le comprimé orodispersible, (0,6 - 5 heures, médiane 3 heures), par rapport au comprimé standard (0,5 - 3 heures, médiane 1,5 heure). Cependant, les concentrations plasmatiques de zolmitriptan sont comparables pour les deux formes, dans les 45 premières minutes qui suivent l'administration, période essentielle pour l'absorption initiale après l'administration.
Populations particulières
La clairance rénale du zolmitriptan et de ses métabolites est réduite (de 7 à 8 fois) chez les patients avec une insuffisance rénale modérée à sévère. Cependant, les AUC du zolmitriptan et du métabolite actif sont légèrement supérieures (16 et 35 %, respectivement) et les demi-vies d'élimination sont légèrement augmentées, soit 3 à 3,5 heures. Ces valeurs restent dans les intervalles observés chez le volontaire sain.
Les données restent insuffisantes chez le sujet âgé de plus de 65 ans.
Dosage
Dosage - ZOLMITRIPTAN - voie orale
Comprimé pelliculé
La dose recommandée de ZOLMITRIPTAN, comprimé pour le traitement d'une crise de migraine est de 2,5 mg.
Si les symptômes de la migraine réapparaissent dans les 24 heures suivant la réponse initiale, une deuxième dose peut être prise. En cas de besoin d'une deuxième dose, celle-ci ne doit pas être prise dans les 2 heures suivant la prise de la première dose. Si un patient n'est pas soulagé après la première dose, il est peu probable qu'une deuxième dose apportera un bénéfice pour la même crise.
Si un patient n'est pas soulagé de façon satisfaisante avec des doses de 2,5 mg, des doses de 5 mg de ZOLMITRIPTAN pourront être envisagées pour les crises suivantes. La prudence est recommandée en raison d'un risque accru d'effet indésirable. La supériorité de la dose de 5 mg comparé à la dose de 2,5 mg n'a pas pu être démontrée lors d'une étude clinique contrôlée. Néanmoins une dose de 5 mg peut être bénéfique pour certains patients.
Il est conseillé de prendre les comprimés de ZOLMITRIPTAN le plus tôt possible dès l'apparition de la céphalée migraineuse. Cependant, ils sont aussi efficaces lorsqu'ils sont administrés plus tard.
En cas de céphalées récurrentes, la dose maximale ne doit pas dépasser 10 mg par 24 heures. Ne pas prendre plus de 2 doses de ZOLMITRIPTAN au cours d'une période de 24 heures.
Utilisation chez les patients âgés de plus de 65 ans
La sécurité d'emploi et l'efficacité du zolmitriptan chez les personnes âgées de plus de 65 ans n'ont pas été établies. Par conséquent, l'utilisation de ZOLMITRIPTAN chez les personnes âgées n'est pas recommandée.
Insuffisants hépatiques
Chez les patients atteints d'insuffisance hépatique légère ou modérée, aucun ajustement de dose n'est nécessaire, toutefois, pour les patients atteints d'insuffisance hépatique grave, la dose maximale de 5 mg en 24 heures est recommandée.
Insuffisants rénaux
Aucun ajustement de dose n'est nécessaire chez les patients dont la clairance de la créatinine est supérieure à 15 ml/mn .
Interactions nécessitant un ajustement de dose
Pour les patients prenant des inhibiteurs de la MAO-A, une dose maximale de 5 mg en 24 heures est recommandée.
Une dose maximale de 5 mg de zolmitriptan en 24 heures est recommandée chez les patients prenant de la cimétidine.
Une dose maximale de 5 mg de zolmitriptan en 24 heures est recommandée chez les patients prenant des inhibiteurs spécifiques du CYP 1A2, comme la fluvoxamine et les quinolones (par exemple, ciprofloxacine).
Utilisation chez l'enfant (de moins de 12 ans)
La sécurité d'emploi et l'efficacité des comprimés de zolmitriptan n'ont pas été évaluées chez les enfants. Par conséquent, l'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les enfants .
Adolescents (de 12 à 17 ans)
L'efficacité des comprimés de ZOLMITRIPTAN n'a pas été démontrée dans un essai clinique contrôlé contre placebo réalisé chez des patients âgés de 12 à 17 ans. Par conséquent, l'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les adolescents de 12 à 17 ans.
Mode d'administration
Le comprimé doit être avalé avec un verre d'eau.
Le zolmitriptan ne devra pas être utilisé à visée prophylactique.
Il est recommandé de prendre le comprimé le plus tôt possible dès l'apparition de la céphalée migraineuse. Cependant, le zolmitriptan est aussi efficace lorsqu'il est administré plus tard.
Le zolmitriptan est inefficace lorsqu'il est administré au moment de l'aura. Il est déconseillé de l'administrer au stade de l'aura.
Posologie
La dose recommandée pour le traitement de la crise de migraine est de un comprimé à 2,5 mg.
Le comprimé orodispersible se dissout rapidement dans la bouche et peut être avalé sans eau, permettant une administration précoce.
Le comprimé orodispersible peut être utilisé lorsqu'une boisson n'est pas disponible, ou pour éviter les nausées et les vomissements qui peuvent accompagner la prise de comprimés avec du liquide.
L'efficacité est significative dans l'heure suivant la prise du comprimé.
Si un patient n'est pas soulagé après la première dose, une seconde dose ne doit pas être prise au cours de la même crise. Le zolmitriptan pourra être utilisé pour la crise suivante.
Toutefois, l'apparition de l'effet pour certains patients peut être retardée en raison de l'absorption plus lente du zolmitriptan sous forme de comprimé orodispersible comparativement au comprimé pelliculé .
Si un patient a été soulagé après la première dose mais que les symptômes de la migraine réapparaissent, un deuxième comprimé peut être pris dans les 24 heures suivantes à condition de respecter un intervalle d'au moins 2 heures entre les 2 prises.
Il est recommandé de ne pas dépasser la dose maximale de 10 mg par 24 heures.
Population pédiatrique
Utilisation chez l'enfant (de moins de 12 ans)
L'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les enfants car la sécurité et l'efficacité des comprimés de zolmitriptan n'ont pas été évaluées chez les enfants de moins de 12 ans.
Adolescents (de 12 à 17 ans)
L'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les adolescents car l'efficacité de zolmitriptan comprimé n'a pas été démontrée dans un essai clinique contrôlée contre placebo, réalisé chez des patients âgés de 12 à 17 ans.
Sujet âgé (de plus de 65 ans)
La sécurité et l'efficacité du zolmitriptan chez le sujet de plus de 65 ans n'ont pas été établies.
Insuffisant hépatique
En cas d'insuffisance hépatique sévère la dose maximale à ne pas dépasser par jour sera de 5 mg. Aucun ajustement posologique n'est nécessaire dans l'insuffisance hépatique légère à modérée.
Insuffisant rénal
Aucun ajustement de dose n'est nécessaire chez les patients ayant une clairance de la créatinine supérieure à 15 ml/min .
Dosage - ZOLMITRIPTAN - application locale en ORL (otorhinolaryngologie)
Solution pour pulvérisation
Le zolmitriptan ne devra pas être utilisé à visée prophylactique.
Il est recommandé de prendre une pulvérisation le plus tôt possible dès l'apparition de la céphalée migraineuse. Cependant, le zolmitriptan est aussi efficace lorsqu'il est administré plus tard.
Le zolmitriptan est inefficace lorsqu'il est administré au moment de l'aura. Il est déconseillé de l'administrer au stade de l'aura.
Adulte :
La dose recommandée pour le traitement de la crise de migraine est de une pulvérisation à 5 mg/0,1 ml.
Le spray nasal est administré en une pulvérisation unique dans une seule narine.
L'efficacité est significative dans les 15 minutes, suivant la pulvérisation.
Le pulvérisateur nasal est particulièrement adapté lorsque la voie orale ne peut être utilisée (patients présentant des nausées et vomissements au cours d'une crise).
Si un patient n'est pas soulagé après la première dose, une seconde dose ne doit pas être prise au cours de la même crise. Le zolmitriptan pourra être utilisé pour la crise suivante.
Si un patient a été soulagé après la première pulvérisation mais que les symptômes de la migraine réapparaissent une deuxième dose peut être prise dans les 24 heures suivantes à condition de respecter un intervalle d'au-moins 2 heures entre les 2 prises.
Il est recommandé de ne pas dépasser la dose maximale de 10 mg par 24 heures.
Utilisation chez l'enfant (de moins de 12 ans)
L'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les enfants car la sécurité et l'efficacité de ZOLMITRIPTAN n'ont pas été évaluées chez les enfants de moins de 12 ans.
Adolescents (de 12 à 17 ans)
L'utilisation de ZOLMITRIPTAN n'est pas recommandée chez les adolescents âgés de 12 à 17 ans car la sécurité et l'efficacité de ZOLMITRIPTAN n'ont pas été évaluées chez les adolescents de 12 à 17 ans.
Sujet âgé (de plus de 65 ans) :
La sécurité et l'efficacité du zolmitriptan chez le sujet de plus de 65 ans n'ont pas été établies.
Insuffisant hépatique :
En cas d'insuffisance hépatique sévère la dose maximale à ne pas dépasser par jour sera de 5 mg. Aucun ajustement posologique n'est nécessaire dans l'insuffisance hépatique légère à modérée.
Insuffisant rénal :
Aucun ajustement de dose n'est nécessaire chez les patients ayant une clairance de la créatinine supérieure à 15 ml/min .
Indications
Indications - ZOLMITRIPTAN - usage systémique
Traitement de la phase céphalalgique de la crise de migraine.
Effets indésirables
Effets indésirables - ZOLMITRIPTAN - usage systémique
Les effets indésirables sont habituellement transitoires, apparaissent en début de traitement et disparaissent spontanément.
Les effets indésirables sont classés par fréquence, en utilisant la classification suivante : très fréquents (≥1/10), fréquents (≥1/100 - <1/10), peu fréquents (≥1/1000 - <1/100), rares (≥1/10000 - <1/1000), très rares (<1/10 000).
Les effets indésirables suivants ont été rapportés après administration de zolmitriptan :
Système classe-organe | Fréquence | Effets indésirables |
Affections du système immunitaire | Rare | Réactions d'hypersensibilité y compris urticaire, angiodème, et reactions anaphylactiques |
Affections du système nerveux | Fréquent | Sensations anormales ou troubles des sensations ; Etourdissements ; Céphalées ; Hyperesthésie ; Paresthésie ; Somnolence ; Sensation de chaleur |
Affections cardiaques | Fréquent | Palpitations |
Peu fréquent | Tachycardie |
Très rare | Infarctus du myocarde ; Angor ; Vasospasme coronarien |
Affections du système vasculaire | Peu fréquent | Augmentations légères de la pression artérielle ; Augmentations transitoires de la pression artérielle systémique |
Affections gastro-intestinales | Fréquent | Douleur abdominale ; Nausée ; Vomissement ; Sécheresse buccale ; Dysphagie |
Très rare | Ischémie ou infarctus (par exemple ischémie intestinale, infarctus intestinal, infarctus splénique) pouvant se presenter sous forme de diarrhée sanglante ou de douleur abdominale |
Affections musculo-squelettiques et systémiques | Fréquent | Faiblesse musculaire ; Myalgie |
Affections du rein et des voies urinaires | Peu fréquent | Polyurie ; Pollakiurie |
Très rare | Miction impérieuse |
Troubles généraux et anomalies au site d'administration | Fréquent | Asthénie ; Lourdeur, sensation d'oppression, douleur ou pression au niveau de la gorge, du cou, des membres ou de la poitrine. |
Certains symptômes peuvent faire partie de la crise de migraine.
Surdosage
Les volontaires sains recevant des doses orales uniques de 50 mg de zolmitriptan présentent fréquemment une sédation.
La demi-vie d'élimination du zolmitriptan étant de 2,5 à 3 heures , en cas de surdosage, la surveillance des patients devra être poursuivie au moins 15 heures ou tant que les signes ou symptômes persistent.
Il n'existe pas d'antidote spécifique du zolmitriptan. En cas d'intoxication sévère, une surveillance intensive est recommandée, en étant particulièrement attentif à la surveillance et au maintien des fonctions ventilatoire et cardio-vasculaire.
L'effet d'une hémodialyse ou d'une dialyse péritonéale sur les concentrations sériques du zolmitriptan est inconnu.
Grossesse/Allaitement
Grossesse
Les études chez l'animal n'ont pas mis en évidence d'effet tératogène. En l'absence d'effet tératogène chez l'animal, un effet malformatif dans l'espèce humaine n'est pas attendu. En effet, à ce jour, les substances responsables de malformations dans l'espèce humaine se sont révélées tératogènes chez l'animal au cours d'études bien conduites sur deux espèces.
Dans l'espèce humaine, il n'existe pas actuellement de données en nombre suffisant pour évaluer un éventuel effet malformatif ou ftotoxique du
zolmitriptan lorsqu'il est administré pendant la grossesse.
En conséquence, par mesure de précaution, il est préférable de ne pas utiliser le zolmitriptan pendant la grossesse.
Allaitement
Chez l'animal, le zolmitriptan est excrété dans le lait.
En l'absence de données spécifiques chez femme allaitante, l'utilisation de zolmitriptan est déconseillée.
Interactions avec d'autres médicaments
Associations contre-indiquées
+ IMAO non sélectif (iproniazide)
Risque d'hypertension artérielle, de vasoconstriction artérielle coronaire.
+ IMAO sélectifs A
Risque d'hypertension artérielle, de vasoconstriction artérielle coronaire.
+ IMAO sélectifs B (sélégiline)
Risque d'hypertension artérielle, de vasoconstriction artérielle coronaire.
+ Linézolide (antibactérien)
Risque d'hypertension artérielle, de vasoconstriction artérielle coronaire.
+ Vasoconstricteurs alcaloïdes de l'ergot de seigle (ergotamine, dihydroergotamine, méthysergide) et autres agonistes des récepteurs 5HT1D.
Les données issues de sujets sains suggèrent une absence d'interaction pharmacocinétique ou d'interaction cliniquement significative entre le
zolmitriptan et l'ergotamine. Toutefois, il existe un risque d'hypertension artérielle, de vasoconstriction artérielle coronaire, et une administration concomittante est contre-indiquée.
Respecter un délai de 24 heures entre l'arrêt de l'alcaloïde et la prise du triptan.
Inversement, il est conseillé d'attendre au moins 6 heures après la prise de zolmitriptan avant d'administrer un médicament contenant de l'ergotamine.
Associations à prendre en compte
+ Antidépresseurs inhibiteurs sélectifs de la recapture sérotonine
Risque potentiel d'hypertension artérielle, de vasoconstriction artérielle coronaire ou de syndrome sérotoninergique.
+ Vasoconstrictions alcaloïdes de l'ergot de seigle (méthylergométrine)
Risque d'hypertension artérielle, de vasoconstriction artérielle coronaire.
L'administration concomitante d'un autre agoniste des récepteurs 5HT1B/1D doit être évitée dans les 24 heures suivant un traitement par CEPHOROMITAN.

 Français
Français Русский
Русский