M05B Médicaments affectant la structure et la minéralisation osseuseFormes pharmaceutiques
- comprimé
- comprimé gastro-résistante
- comprimé pelliculé
Pharmacodynamique
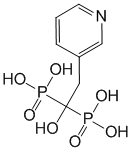
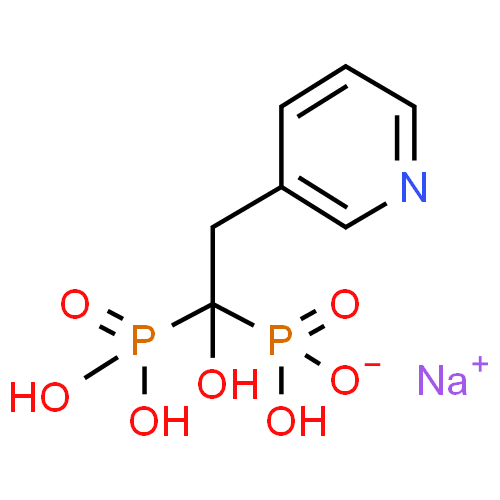
Le risédronate monosodique est un pyridinil bisphosphonate qui se fixe sur l'hydroxyapatite osseuse et inhibe la résorption osseuse induite par l'ostéoclaste. Le remodelage osseux est réduit alors que l'activité ostéoblastique et la minéralisation osseuse sont préservées. Dans les études précliniques, le risédronate monosodique a révélé une puissante activité anti-résorptive et anti-ostéoclastique, et a augmenté, de façon dose-dépendante, la masse osseuse et la force biomécanique du squelette. L'activité du risédronate monosodique a été confirmée en mesurant les marqueurs biochimiques du remodelage osseux lors d'études pharmacodynamiques et cliniques. Dans les études chez des femmes ménopausées, les diminutions des marqueurs biochimiques du remodelage osseux ont été observées en 1 mois de traitement et ont atteint un pic maximal en 3 à 6 mois. Les diminutions des marqueurs biochimiques du remodelage osseux ont été similaires avec Risédronate 35 mg une fois par semaine et Risédronate 5 mg/jour à 12 mois. Dans une étude chez des hommes ostéoporotiques, les diminutions des marqueurs biochimiques du remodelage osseux ont été observées au plus tôt après 3 mois de traitement, et se sont maintenues jusqu'au 24ème mois. Traitement de l'ostéoporose postménopausique Un nombre de facteurs de risque est fréquemment associé au développement de l'ostéoporose postménopausique: masse osseuse basse, densité minérale osseuse basse, ménopause précoce, antécédent de tabagisme, antécédent familial d'ostéoporose. La fracture est la conséquence clinique de l'ostéoporose. Le risque de fracture s'accroît avec le nombre de facteurs de risque.
Pharmacocinétique
Pharmacocinétique - ACIDE RISÉDRONIQUE - voie orale
Absorption
L'absorption après une prise orale est relativement rapide (tmax ≃ 1 heure) et indépendante des doses étudiées (étude en prise unique: de 2,5 à 30 mg; études avec des prises multiples: de 2,5 à 5 mg/jour et jusqu'à 50 mg, une fois par semaine). La biodisponibilité orale moyenne du comprimé est de 0,63 % mais elle diminue en cas de prise alimentaire concomitante. La biodisponibilité est identique chez les hommes et les femmes.
Distribution
Le volume de distribution moyen à l'état d'équilibre est de 6,3 l/kg chez l'homme. Le taux de liaison aux protéines plasmatiques est de l'ordre de 24 %.
Biotransformation
Aucun signe de métabolisme systémique du risédronate monosodique n'a été retrouvé.
Élimination
Environ 50 % d'une dose orale de risédronate monosodique est éliminée dans les urines en 24 heures et 85 % d'une dose intraveineuse sont retrouvés dans les urines 28 jours après. La clairance rénale moyenne est de 105 ml/min et la clairance totale moyenne est de 122 ml/min, la différence étant probablement due à une adsorption osseuse. La clairance rénale ne dépend pas de la concentration; une relation linéaire entre la clairance rénale et la clairance de la créatinine a été retrouvée. Le risédronate monosodique non absorbé est éliminé tel quel dans les selles. Après administration orale, le profil de concentration plasmatique montre une élimination en fonction du temps en trois phases, avec une demi-vie finale de 480 heures.
Populations particulières:Sujets âgés: un ajustement posologique n'est pas nécessaire.
Utilisateurs d'acide acétylsalicylique/AINS: Parmi les utilisateurs réguliers d'acide acétylsalicylique ou d'AINS (> 3 jours par semaine), l'incidence des effets indésirables de type gastro-intestinal supérieur est identique chez les patients traités par risédronate monosodique et les sujets contrôle.
Dosage
Dosage - ACIDE RISÉDRONIQUE - voie orale
Comprimé pelliculé
Chez l'adulte, la dose recommandée est d'un comprimé à 35 mg, une fois par semaine, par voie orale. Le comprimé doit être pris le même jour de la semaine, chaque semaine.
Mode d'administration
Voie orale.
L'alimentation interfère avec l'absorption du risédronate monosodique. Afin d'obtenir une absorption optimale, les patients doivent prendre ACIDE RISÉDRONIQUE :
Avant le petit déjeuner : au moins 30 minutes avant l'absorption des premiers aliments, des autres médicaments ou boissons (autres que de l'eau plate) de la journée.
Les patients doivent être informés que s'ils oublient une prise de ACIDE RISÉDRONIQUE 35 mg, ils doivent la prendre le jour où ils s'en aperçoivent. Ensuite, ils doivent revenir à la prise hebdomadaire du comprimé en se basant sur le jour choisi initialement. Ils ne doivent pas prendre deux comprimés le même jour.
Le comprimé doit être avalé entier, sans être croqué et sans le laisser fondre dans la bouche.
Le comprimé de ACIDE RISÉDRONIQUE doit être avalé en position assise ou debout, avec un grand verre d'eau plate (≥120 ml), pour faciliter le transit jusqu'à l'estomac.
Les patients ne doivent pas s'allonger au cours des 30 minutes qui suivent la prise du comprimé . Une supplémentation en calcium et en vitamine D sera à envisager si l'apport alimentaire est insuffisant.
Sujets âgés :
Aucun ajustement de la posologie n'est nécessaire car la biodisponibilité, la distribution et l'élimination sont identiques chez les sujets âgés (>60 ans) et chez les sujets plus jeunes. Ceci a été démontré également chez les patientes ménopausées très âgées de 75 ans et plus.
Insuffisants rénaux :
Aucune modification de posologie n'est nécessaire chez les patients ayant une insuffisance rénale légère à modérée. L'utilisation du risédronate monosodique est contre-indiquée chez les patients ayant une insuffisance rénale sévère (clairance de la créatinine <30 ml/min) .
Population pédiatrique :
Le risédronate monosodique n'est pas recommandé chez les enfants et les adolescents de moins de 18 ans en raison de l'insuffisance de données de sécurité et d'efficacité .
La durée optimale du traitement par bisphosphonates pour l'ostéoporose n'a pas été établie. La nécessité de poursuivre le traitement doit être réévaluée régulièrement au cas par cas en fonction des bénéfices et des risques potentiels de ACIDE RISÉDRONIQUE, particulièrement après 5 ans ou plus de traitement.
Indications
Indications - ACIDE RISÉDRONIQUE - usage systémique
Traitement de l'ostéoporose post-ménopausique pour réduire le risque de fractures vertébrales. Traitement de l'ostéoporose post-ménopausique avérée, pour réduire le risque de fractures de hanche .
Traitement de l'ostéoporose chez l'homme à haut risque de fractures .
Contre-indications
Hypersensibilité connue à la substance active ou à l'un des excipients.
Hypocalcémie .
Grossesse et allaitement.
Insuffisance rénale sévère (clairance de la créatinine < 30 ml/min).
Effets indésirables
Effets indésirables - ACIDE RISÉDRONIQUE - usage systémique
Le risédronate monosodique a été étudié lors d'essais cliniques de phase III ayant inclus plus de 15 000 patients. Dans ces essais cliniques, la majorité des effets indésirables a été d'intensité légère à modérée et n'a généralement pas nécessité l'interruption du traitement. Les évènements indésirables rapportés dans les essais cliniques de phase III chez les femmes ménopausées ostéoporotiques traitées jusqu'à 36 mois par risédronate monosodique 5 mg/j (n = 5020) ou placebo (n = 5048) et considérés comme possiblement ou probablement liés au risédronate monosodique sont listés ci-dessous en utilisant la convention suivante (incidence des évènements indésirables versus placebo notée entre parenthèse): très fréquents (≥ 1/10), fréquents (≥ 1/100; < 1/10), peu fréquents (≥ 1/1000; < 1/100), rares (≥ 1/10000; < 1/1000), très rares (< 1/10000), inconnu (la fréquence ne peut être estimée à partir des données disponibles).
Troubles du système nerveux central Fréquents: maux de tête (1,8 % vs 1,4 %)
Troubles oculaires Peu fréquents: Iritis*
Troubles gastro-intestinaux Fréquents: constipation (5,0 % vs 4,8 %), dyspepsie (4,5 % vs 4,1 %), nausées (4,3 % vs 4,0 %), douleurs abdominales (3,5 % vs 3,3 %), diarrhées (3,0 % vs 2,7 %) Peu fréquents: gastrite (0,9% vs 0,7%), sophagite (0,9 % vs 0,9 %), dysphagie (0,4 % vs 0,2 %), duodénite (0,2 % vs 0,1 %), ulcère sophagien (0,2 % vs 0,2 %) Rares: Glossite (< 0,1 % vs 0,1 %), sténose de l'sophage (< 0,1 % vs 0,0 %).
Troubles musculo-squelettiques et des tissus conjonctifs Fréquents: douleurs musculo-squelettiques (2,1 % vs 1,9 %)
Explorations (hepatobilaire) Rares: anomalie des tests hépatiques*
Examens biologiques Une diminution précoce, transitoire, modérée et asymptomatique des taux plasmatiques de calcium et phosphate a été observée chez certains patients. *Incidence non significative dans les études de phase III sur l'ostéoporose; fréquence basée sur les effets indésirables, les examens de laboratoire et les résultats du rechallenge dans les essais cliniques précoces. Dans une étude multicentrique, en double aveugle, sur un an, comparant le risédronate monosodique 5 mg en prise quotidienne (n = 480) et le risédronate monosodique 35 mg en prise hebdomadaire (n = 485) chez les femmes ménopausées ostéoporotiques, les profils globaux de tolérance et de sécurité d'emploi ont été similaires. Les effets indésirables suivants, considérés comme possiblement ou probablement liés au produit par les investigateurs, ont été rapportés (incidence supérieure dans le groupe risédronate monosodique 35 mg comparé au groupe risédronate monosodique 5 mg): troubles gastro-intestinaux (1,6 % vs. 1,0 %) et douleurs (1,2 % vs. 0,8 %). Dans une étude de 2 ans chez des hommes ostéoporotiques, le profil global de sécurité et de tolérance était similaire entre les groupes traités par risédronate monosodique et par placebo. Les effets indésirables étaient comparables à ceux observés précédemment chez les femmes. De plus, les effets indésirables additionnels suivants ont été rapportés depuis la commercialisation (fréquence inconnue):
Troubles du système immunitaire Réaction anaphylactique
Troubles visuels Iritis, uvéite
Troubles hépato-biliaires Troubles hépatiques graves. Dans la plupart des cas rapportés, les patients étaient également traités avec d'autres médicaments connus pour causer des troubles hépatiques.
Atteinte de la peau et des tissus sous-cutanés Hypersensibilité et réactions cutanées, incluant angio-dème, rash généralisé et réactions cutanées bulleuses, parfois sévères incluant des cas isolés de syndrome de Stevens-Johnson, de nécrolyse épidermique toxique et de vascularite leucocytoclasique. Alopécie
Troubles musculo-squelettiques et des tissus conjonctifs Ostéonécrose de la mâchoire. Fractures fémorales atypiques sous-trochantériennes et diaphysaires (effets indésirables de classe des bisphosphonates) (fréquence rare).
Surdosage
Aucune information spécifique sur le traitement d'un surdosage en risédronate monosodique n'est actuellement disponible.
A la suite d'un surdosage important, une diminution de la calcémie peut être observée. Chez certains patients, des signes et symptômes d'hypocalcémie peuvent également être observés.
Afin de fixer le risédronate monosodique et de réduire son absorption, du lait ou des anti-acides contenant du magnésium, du calcium ou de l'aluminium doivent être administrés. En cas de surdosage important, un lavage gastrique peut être envisagé afin d'éliminer le risédronate monosodique non absorbé.
Grossesse/Allaitement
Il n'y a pas de données disponibles sur l'utilisation du risédronate monosodique chez la femme enceinte. Des études chez l'animal ont montré une toxicité sur la fonction de reproduction . Le risque potentiel chez les femmes n'est pas connu. Les études chez l'animal ont montré qu'une petite quantité de risédronate monosodique passait dans le lait.
Le risédronate monosodique ne doit pas être utilisé chez la femme enceinte ou qui allaite.
Interactions avec d'autres médicaments
Aucune étude spécifique d'interactions n'a été réalisée. Cependant aucune interaction médicamenteuse cliniquement pertinente n'a été retrouvée pendant les essais cliniques.
Respectivement 33 % et 45 % des patientes ayant participé aux études de Phase III dans l'ostéoporose avec le risédronate monosodique en prise quotidienne, ont utilisé de l'aspirine ou des AINS.
Dans les études de phase III du risédronate monosodique en prise hebdomadaire, respectivement 57 % et 40 % des patientes ont utilisé de l'aspirine ou des AINS.
Parmi les utilisateurs réguliers d'acide acétylsalicylique ou d'AINS (≥ 3 jours par semaine), l'incidence des effets secondaires digestifs hauts est identique chez les patients traités par risédronate monosodique et les sujets contrôle.
Si nécessaire, le risédronate monosodique peut être utilisé en association à un traitement strogénique substitutif (pour les femmes uniquement).
Une ingestion concomitante de médicaments contenant des cations polyvalents (tels que calcium, magnésium, fer et aluminium) peuvent interférer avec l'absorption du risédronate monosodique .
Le risédronate monosodique n'est pas métabolisé, n'entraîne pas d'induction enzymatique au niveau du cytochrome P450 et a un faible taux de fixation aux protéines.

 Français
Français Русский
Русский