Pharmacodynamique
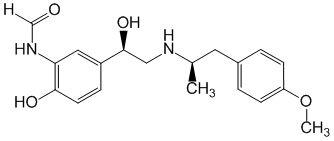
Le formotérol est un stimulant bêta‑2 sélectif puissant. Après inhalation, il exerce un effet bronchodilatateur grâce à une action stimulante sur les récepteurs bêta-2 du muscle lisse bronchique chez les patients présentant une obstruction des voies aériennes réversible.
Après inhalation d'une dose unique il entraîne une bronchodilatation rapide (1 à 3 minutes), maximum en 2 heures, persistant environ 12 heures. Aux doses thérapeutiques, les effets cardiovasculaires sont minimes et occasionnels.
Le formotérol inhibe la libération de l'histamine et des leucotriènes à partir des cellules pulmonaires humaines sensibilisées passivement. Des expérimentations animales ont mis en évidence certaines propriétés anti-inflammatoires, telles une inhibition de l'dème et de l'accumulation de cellules inflammatoires.
Chez l'Homme, le formotérol a montré son efficacité dans la prévention du bronchospasme induit par les allergènes inhalés, l'exercice physique, l'air froid, l'histamine ou la méthacholine.
Chez des patients souffrant de bronchopneumopathie chronique obstructive, le formotérol aux doses de 12 ou 24 mcg à raison de 2 fois par jour a permis d'obtenir un effet bronchodilatateur rapide chez les patients souffrant d'une BPCO stable qui persistait plus de 12 heures. Il a été montré que la qualité de vie de ces patients était améliorée par le traitement (St George Respiratory Questionnaire).
Pharmacocinétique
Pharmacocinétique - FORMOTÉROL - voie inhalée
Le formotérol agissant localement au niveau du poumon, les taux plasmatiques ne sont pas corrélés à l'effet thérapeutique. Aux doses thérapeutiques, les concentrations plasmatiques du formotérol, après inhalation, sont inférieures aux limites de sensibilité des méthodes d'analyse.
Absorption
Le formotérol est rapidement absorbé après inhalation. Les pics plasmatiques sont atteints 10 minutes environ après l'inhalation. Il est probable que la majeure partie du formotérol administré soit dégluti et donc absorbé au niveau du tractus digestif.
Distribution et biotransformation
La liaison aux protéines plasmatiques est de 61 à 64 % (albumine: 34 %).Le formotérol est essentiellement métabolisé par glucuronisation directe et est entièrement éliminé. Une autre voie de métabolisation consiste en une O-déméthylation suivie d'une glucuronisation puis élimination complète. Plusieurs enzymes sont responsables de la glucuronisation et de l'O-déméthylation du formotérol suggérant ainsi un faible risque d'interaction médicamenteuse due à l'inhibition d'une isoenzyme spécifique impliquée dans le métabolisme du formotérol.
Aux doses thérapeutiques, le formotérol n'inhibe pas les isoenzymes du cytochrome P450.
La clairance plasmatique totale et le volume de distribution n'ont pas été déterminés.
Élimination
La substance active et ses métabolites sont entièrement éliminés, les deux tiers d'une dose orale étant éliminés dans les urines et un tiers dans les selles. La clairance rénale du formotérol est de 150 ml/min.
La majeure partie d'une dose de formotérol est éliminée par métabolisation. Après inhalation, 6 à 9 % de la dose (en moyenne) sont éliminés sous forme inchangée dans les urines. Près de 20 % d'une dose intraveineuse sont excrétés sous forme intacte dans les urines. La demi-vie terminale après inhalation est estimée à 17 heures.
Populations spécifiques
Le retentissement d'une diminution de la fonction rénale ou hépatique sur la pharmacocinétique du formotérol chez le sujet âgé n'est pas connu. Compte-tenu du métabolisme essentiellement hépatique du formotérol, une diminution de l'exposition systémique est attendue chez les patients insuffisants hépatiques sévères.
Dosage
Dosage - FORMOTÉROL - voie inhalée
Solution pour inhalation
La posologie est fonction de la sévérité de la maladie.
Le médicament ne devra pas être utilisé plus de 3 mois après la date de dispensation au patient par le pharmacien .
Bien que FORMOTÉROL agisse rapidement, c'est un bronchodilatateur inhalé de longue durée d'action et il doit, par conséquent, être réservé au traitement régulier continu.
Posologie dans le traitement de l'asthme
Adultes (y compris les sujets âgés) et adolescents âgés de 12 ans et plus:
Dose usuelle: une bouffée matin et soir (soit 24 mcg de fumarate de formotérol dihydraté par jour).
Dans les cas sévères: jusqu'à deux bouffées matin et soir au maximum (soit 48 mcg de fumarate de formotérol dihydraté par jour).
La dose journalière maximale est de 4 bouffées (48 mcg de fumarate de formotérol dihydraté).
FORMOTÉROL ne constitue pas le traitement de la crise d'asthme aiguë.
Pour le traitement des crises aiguës d'asthme, il est recommandé d'avoir recours à un bronchodilatateur β2 mimétique par voie inhalée de courte durée d'action.
Les patients devront être avertis de ne pas arrêter ou modifier leur corticothérapie lors de l'instauration du traitement par FORMOTÉROL.
La persistance ou l'augmentation des symptômes ou leur contrôle insuffisant avec les doses recommandées de FORMOTÉROL témoignent d'une instabilité de la maladie sous jacente.
Bronchopneumopathie chronique obstructive (BPCO)
Adulte (âgés de 18 ans et plus)
La dose usuelle est de 1 inhalation 2 fois par jour (1 inhalation le matin et 1 inhalation le soir, soit 24 mcg de fumarate de formotérol par jour).
En traitement continu, la dose journalière ne doit pas dépasser 2 inhalations.
Si besoin, des inhalations supplémentaires peuvent néanmoins être prises occasionnellement pour soulager les symptômes, sans toutefois dépasser une dose totale maximum de 4 inhalations par jour (traitement continu et inhalations supplémentaires comprises). Ne pas dépasser plus de 2 inhalations à chaque prise.
Insuffisance hépatique et rénale
Il n'a pas été réalisée d'étude clinique dans ces populations, néanmoins, les données existantes ne suggèrent pas la nécessité d'un ajustement de la posologie en cas d'insuffisance rénale ou hépatique.
Mode d'emploi
Afin de limiter le risque d'erreur de manipulation du dispositif par le patient, il est utile que le médecin ou un professionnel de santé s'assure que celui-ci utilise correctement l'inhalateur.
Avant la première utilisation de l'inhalateur et après trois jours ou plus de non utilisation, une bouffée sera libérée dans l'air pour assurer le bon fonctionnement du dispositif.
Dans la mesure du possible, les patients doivent être en position verticale, debout ou assis, quand ils actionnent l'inhalateur.
1. Retirer le capuchon protecteur de l'embout buccal.
2. Expirer hors du dispositif aussi profondément que possible.
3. Tenir la cartouche verticalement, en dirigeant le fond vers le haut, et introduire l'embout buccal entre les lèvres bien serrées.
4. Inspirer profondément par la bouche tout en appuyant sur le fond de la cartouche (en haut) afin de libérer une bouffée.
5. Retenir son souffle aussi longtemps que possible sans effort et, pour terminer, retirer l'inhalateur de la bouche.
Si une autre bouffée doit être inhalée, maintenir l'inhalateur en position verticale pendant environ 30 secondes puis répéter les étapes 2 à 5.
Toujours refermer après emploi à l'aide du capuchon protecteur.
IMPORTANT: les étapes 2 à 4 ne doivent pas être effectuées trop rapidement.
Si une partie du gaz s'échappe de la partie supérieure de l'inhalateur ou du côté de l'embout buccal, recommencez à partir de l'étape 2.
Chez les patients dont la capacité de préhension est défaillante, l'inhalateur sera tenu avec les deux mains. Dans ce cas, la partie supérieure de l'inhalateur sera maintenue entre les deux index et la partie inférieure entre les deux pouces.
En cas de difficulté pour le patient de synchroniser l'inspiration avec le déclenchement de l'appareil, une chambre d'inhalation devra être utilisée. Néanmoins, aucune donnée clinique n'est disponible concernant l'emploi de FORMOTÉROL avec une chambre d'inhalation.
Voie inhalée.
La prise de doses supplémentaires par rapport à la posologie usuelle plus de 2 jours par semaine, est le signe d'un contrôle insuffisant et le traitement de fond doit alors être réévalué.
Le traitement sera administré en 2 prises par jour.
ASTHME :
Adultes (y compris les personnes âgées) et adolescents de plus de 12 ans :
La posologie usuelle est de 1 inhalation (12 mcg) 2 fois par jour. Pour les asthmes sévères, la posologie peut être augmentée jusqu'à 2 inhalations (24 mcg) 2 fois par jour.
La dose maximale journalière est de 4 inhalations (2 inhalations 2 fois par jour) correspondant à 48 mcg.
Population pédiatrique
Enfants 6 ans et plus :
La posologie usuelle est de 1 inhalation (12 mcg) 2 fois par jour. Pour les asthmes sévères, la posologie peut être augmentée jusqu'à 2 inhalations (24 mcg) 2 fois par jour, après évaluation par le médecin.
En traitement régulier continu, la dose journalière à ne pas dépasser est de 2 inhalations (24 mcg). Toutefois, de façon occasionnelle, elle pourra être portée à 4 inhalations réparties sur une période de 24 heures.
Enfants de moins de 6 ans :
AsmelorNovolizer n'est pas recommandé chez l'enfant de moins de 6 ans en raison de l'insuffisance de données dans cette tranche d'âge.
BRONCHOPNEUMOPATHIE CHRONIQUE OBSTRUCTIVE (BPCO) :
Adultes (y compris les personnes âgées) et adolescents de plus de 12 ans :
La posologie usuelle en traitement régulier continu est de 1 inhalation (12 mcg) deux fois par jour.
La dose journalière usuelle à ne pas dépasser en traitement régulier continu est de 2 inhalations (24 mcg). Toutefois, si besoin, des inhalations supplémentaires à la posologie usuelle prescrite dans le cadre du traitement régulier continu peuvent être prises pour soulager les symptômes, sans toutefois dépasser la dose totale maximale de 4 inhalations par jour (soit 48 mcg pour le traitement continu et les inhalations supplémentaires comprises). A chaque prise, ne pas dépasser plus de 2 inhalations.
Le formotérol inhalé est indiqué chez les patients recevant une corticothérapie inhalée lorsqu'un traitement symptomatique continu de l'asthme est nécessaire en plus du corticoïde inhalé.
Bien que le formotérol ait un délai d'action rapide, il convient de réserver l'utilisation des bronchodilatateurs inhalés de longue durée d'action (tel que le formotérol) pour le traitement symptomatique continu de fond seulement en prise régulière.
Le formotérol n'est pas destiné au traitement des crises d'asthme. En cas de crise d'asthme, un agoniste β2 de courte durée d'action doit être utilisé.
Les patients doivent être avertis de ne pas arrêter ou modifier leur traitement corticoïde associé lorsque le traitement par FORMOTÉROL est instauré.
Sujets âgés et patients présentant une insuffisance rénale ou hépatique
Aucun ajustement posologique n'est nécessaire chez les patients âgés ou les insuffisants rénaux ou hépatiques .
Mode d'administration
Modalités du traitement
Afin d'assurer une diffusion intrabronchique optimale du principe actif, l'inhalation devra être réalisée avec un flux régulier en inspirant aussi profondément et rapidement que possible (jusqu'à l'amplitude d'inspiration maximale). Le dispositif est muni d'un système signalant par un déclic audible et un changement de couleur de la fenêtre de contrôle si l'inhalation a été effectuée correctement.
Si le dispositif ne signale pas par un déclic et un changement de couleur de la fenêtre de contrôle que l'inhalation a été réalisée correctement, le patient devra renouveler l'inhalation.
L'inhalateur reste bloqué jusqu'à ce que l'inhalation soit effectuée correctement.
Instructions pour l'utilisation et la manipulation du Novolizer
Rechargement
Appuyer légèrement sur les surfaces nervurées situées des 2 côtés du couvercle, pousser celui-ci vers l'avant et le retirer.
Retirer le film protecteur en aluminium du boîtier de la cartouche et prélever une cartouche neuve.
Insérer la cartouche dans le Novolizer, en orientant le compteur de doses face à l'embout buccal.
Replacer le couvercle dans ses guides latéraux et le pousser horizontalement vers le bouton jusqu'à ce qu'il s'insère dans son logement. La cartouche peut être laissée dans l'inhalateur Novolizer jusqu'à ce qu'elle soit vide ou durant 6 mois au maximum après insertion.
Remarque : Les cartouches d'FORMOTÉROL 12 mcg ne peuvent être utilisées qu'avec l'inhalateur de poudre NOVOLIZER.
Mode d'emploi du dispositif
1. Pour l'inhalation, il est préférable d'être assis ou debout. Lors de l'utilisation du dispositif Novolizer, toujours tenir ce dernier horizontalement. D'abord retirer le capuchon protecteur.
2. Appuyer à fond sur le bouton coloré. On perçoit alors un double déclic sonore et la couleur de la fenêtre de contrôle (en bas) passe du rouge au vert. Ensuite, relâcher le bouton coloré. La couleur verte dans la fenêtre indique que le Novolizer est prêt à l'emploi.
3. Expirer à fond (hors de l'inhalateur).
4. Fermer les lèvres autour de l'embout buccal. Inhaler la poudre fermement, profondément et aussi rapidement que possible (jusqu'à l'inhalation complète). Pendant cette inhalation, on doit entendre un déclic sonore prouvant que l'inhalation a été correctement effectuée. Retenir sa respiration pendant quelques secondes puis respirer normalement.
Remarque : Si le patient a besoin de plusieurs inhalations, répéter les étapes 2 à 4.
5. Replacer le capuchon protecteur sur l'embout buccal. L'inhalation est maintenant terminée.
6. Le chiffre qui apparaît dans la fenêtre supérieure indique le nombre de doses restantes, de 10 en 10 de 60 à 0 doses restantes.
Remarque : Il ne faut appuyer sur le bouton coloré qu'immédiatement avant l'inhalation.
Avec le dispositif Novolizer, l'inhalation involontaire d'une double dose est impossible. Le clic sonore et le changement de couleur dans la fenêtre de contrôle indiquent que l'inhalation a été effectuée correctement. Si la couleur de la fenêtre de contrôle demeure inchangée, il faut recommencer l'inhalation. Si l'inhalation n'est pas effectuée correctement après plusieurs tentatives, le patient doit consulter son médecin.
Nettoyage
Le dispositif NOVOLIZER doit être nettoyé à intervalles réguliers et au minimum lors de chaque changement de cartouche. Pour connaître les instructions concernant le nettoyage de l'appareil, se référer à la notice d'utilisation contenue dans la boîte.
Remarque : afin d'assurer une utilisation correcte de l'inhalateur, il convient d'expliquer clairement aux patients le mode d'emploi de l'appareil. Lors de l'utilisation de ce médicament chez l'enfant, il conviendra de s'assurer qu'un adulte surveille l'administration du médicament.
Poudre pour inhalation en gélule
L'utilisation par le patient de doses supérieures à la posologie usuelle sur plus de 2 jours par semaine
est le signe d'un contrôle insuffisant de la maladie et doit conduire à une réévaluation du traitement.
FORMOTÉROL n'est pas recommandé chez les enfants de moins de 6 ans en raison de l'insuffisance de données de sécurité et d'efficacité.
Asthme
Dans l'asthme, FORMOTÉROL peut être utilisé régulièrement à raison de une ou deux prises quotidiennes, et aux moments où surviennent des symptômes broncho-obstructifs aigus pour les soulager.
Adultes (au-dessus de 18 ans) :
Traitement des symptômes broncho-obstructifs aigus : 1 inhalation.
Traitement symptomatique continu : dose usuelle : 1 inhalation une ou deux fois par jour.
Certains patients peuvent nécessiter jusqu'à 2 inhalations une ou deux fois par jour.
Prévention de l'asthme induit par l'effort : 1 inhalation avant l'effort.
En traitement continu, la dose journalière à ne pas dépasser est de 4 inhalations, toutefois, de façon
occasionnelle, elle pourra être portée à 6 inhalations par jour réparties sur une période de 24 heures.
A chaque prise, ne pas dépasser 3 inhalations.
Enfants et adolescents, (6 ans et plus) :
Traitement des symptômes broncho-obstructifs aigus : 1 inhalation.
Traitement symptomatique continu: dose usuelle : 1 inhalation une ou deux fois par jour.
Prévention de l'asthme induit par l'effort : 1 inhalation avant l'effort.
En traitement continu, la dose journalière à ne pas dépasser est de 2 inhalations, toutefois, de façon
occasionnelle, elle pourra être portée à 4 inhalations par jour réparties sur une période de 24 heures.
A chaque prise, ne pas dépasser 1 inhalation.
Bronchopneumopathie chronique obstructive
Traitement symptomatique continu : 1 inhalation une ou deux fois par jour.
La dose journalière à ne pas dépasser en traitement continu est de 2 inhalations.
Si besoin, des inhalations supplémentaires à la posologie usuelle prescrite dans le cadre du traitement continu peuvent être prises pour soulager les symptômes, sans toutefois dépasser une dose totale maximum de 4 inhalations par jour (traitement continu et inhalations supplémentaires comprises). A chaque prise, ne pas dépasser plus de 2 inhalations.
Populations spécifiques :
Aucun ajustement posologique n'est nécessaire, chez les patients âgés. Il n'y a pas de données disponibles sur l'utilisation de FORMOTÉROL chez les patients présentant une insuffisance
hépatique ou rénale .
Mode d'emploi du dispositif :
Le fonctionnement du dispositif de FORMOTÉROL est lié à l'inspiration: la poudre contenant le
formotérol est délivrée dans les voies aériennes lorsque le patient inspire au travers de l'embout buccal du dispositif.
Remarque: il est important d'expliquer au patient la nécessité :
d'inspirer à fond au travers de l'embout buccal pour assurer la diffusion optimale de la poudre
dans les voies aériennes,
de ne pas mâcher ni mordre l'embout et de ne pas utiliser l'inhalateur s'il a été endommagé ou si l'embout buccal a été détaché.
Il convient d'informer le patient sur le fait que la quantité de produit délivrée au cours de l'inhalation
étant très faible, l'administration ou le goût ne sont le plus souvent pas perçus.
Des instructions détaillées concernant le mode d'emploi sont fournies avec chaque inhalateur.
Indications
Indications - FORMOTÉROL - voie inhalée
Traitement symptomatique continu de l'asthme :
chez des patients nécessitant des prises quotidiennes de bêta‑2 agonistes à action rapide et de courte durée ;
et/ou en cas de symptômes nocturnes ;
en association avec un traitement anti-inflammatoire continu comme les corticoïdes inhalés ;
Traitement préventif de l'asthme induit par l'effort.
N.B. : le formotérol n'est pas un traitement de la crise d'asthme. En cas de crise d'asthme, utiliser un bêta‑2 mimétique d'action rapide et de courte durée par voie inhalée ou en fonction de la gravité par voie injectable ;
Traitement symptomatique de l'obstruction bronchique au cours de la bronchopneumopathie chronique obstructive.
Cette spécialité est particulièrement adaptée aux sujets chez qui il a été mis en évidence une mauvaise synchronisation main/poumon nécessaire pour une utilisation correcte des aérosols doseurs classiques sans chambre d'inhalation.
Effets indésirables
Effets indésirables - FORMOTÉROL - voie inhalée
Les effets indésirables les plus fréquemment rapportés pour les bêta-2 agonistes tels que les tremblements et les palpitations, sont plutôt modérés et disparaissent après quelques jours de traitement.
Un excipient, le lactose, contient de petites quantités de protéines de lait, ce qui peut provoquer des réactions allergiques.
Exacerbations sévères de l'asthme
Des études cliniques contrôlées contre placebo, menées chez des patients traités par formotérol, pendant au moins 4 semaines, ont montré une augmentation de l'incidence des exacerbations sévères dans le groupe traité par formotérol, particulièrement chez les enfants âgés de 5 à 12 ans (0,9 % pour une dose de 10 à 12 mcg 2 fois/jour - 1,9 % pour une dose de 24 mcg 2 fois/jour) par rapport au groupe de patients sous placebo (0,3%).
Expérience clinique chez l'adolescent et l'adulte asthmatiques :
Dans 2 études pivot contrôlées menées pour un enregistrement aux Etats-Unis, incluant un effectif total de 1095 patients de 12 ans et plus, des exacerbations sévères (aggravation aiguë de l'asthme menant à l'hospitalisation) sont survenues plus fréquemment dans le groupe de patients sous formotérol, 24 mcg 2 fois/jour (9/271 - 3,3 %) que dans le groupe de patients sous formotérol, 12 mcg 2 fois/jour (1/275 - 0,4 %), le groupe placebo (2/277 ‑ 0,7 %) ou le groupe salbutamol (21272 - 0,7 %). Les patients ne recevaient pas de traitement corticoïdes concomitants.
Une étude complémentaire a été ensuite menée chez 2085 patients afin de comparer la survenue d'événements indésirables graves liés à l'asthme dans chacun des groupes (faible et forte dose de formotérol). Les résultats de cette étude de 16 semaines n'ont pas montré de relation dose-effet Le pourcentage de patients ayant présenté des exacerbations sévères dans cette étude a été un peu plus élevé dans le groupe formotérol que dans le groupe placebo (pour les 3 groupes traités en double aveugle : formotérol 24 mcg 2 fois/jour (2/527 - 0,4 %), formotérol 12 mcg 2 fois/jour (3/527 - 0,6 %) et placebo (1/514 - 0,2 %) et pour le groupe traité en ouvert : formotérol 12 mcg 2 fois/jour et jusqu'à 2 inhalations supplémentaires (1/517 - 0,2 %).
Population pédiatrique : Expérience clinique chez l'enfant asthmatique âgé de 5 à 12 ans :
La tolérance de formotérol 12 mcg 2 fois/jour versus 24 mcg 2 fois/jour et le placebo a été évaluée dans une large étude clinique multicentrique, randomisée en double aveugle, de 52 semaines incluant 518 enfants asthmatiques (5 à 12 ans) nécessitant un traitement quotidien par bronchodilatateur et anti-inflammatoire. Les enfants sous formotérol 24 mcg 2 fois/jour (11/171 - 6,4 %) et formotérol 12 mcg 2 fois/jour (8/171 - 4,7 %) ont eu plus d'exacerbations sévères que les enfants ayant reçu le placebo (0/176 0 %).
FORMOTÉROL ne doit pas être administré chez l'enfant de moins de 6 ans en raison de l'absence de données cliniques suffisantes pour cette population.
Tableau récapitulatif des effets indésirables
Les effets indésirables liés à la prise de formotérol (Tableau 1) sont listés selon la terminologie MedDRA par classe de systèmes d'organes. La version de MedDRA utilisée est la version 15.1. Dans chaque classe de systèmes d'organes, les effets indésirables sont rangés par fréquence, du plus fréquent au moins fréquent. A l'intérieur de chaque groupe de fréquence, les effets indésirables sont présentés selon un ordre décroissant de gravité. Les catégories de fréquence sont basées sur la convention suivantes (CIOMS III) : très fréquent (≥ 1/10), fréquent (≥ 1/100 et < 1/10), peu fréquent (≥1/1 000 et < /100), rare (≥1/10 000 et < 1/1 000), très rare (< 1/10 000), cas isolés inclus.
Tableau 1. Effets indésirables issus des études cliniques et provenant d'autres sources
Affections du système immunitaire : |
Rare : | réaction d'hypersensibilité (incluant hypotension, bronchospasme, urticaire, angio‑dème, angio, prurit, rash, réactions cutanées) |
Troubles du métabolisme et de la nutrition : |
Rare : | hypokaliémie |
Très rare : | hyperglycémie |
Affections psychiatriques : |
Peu fréquent : | agitation (incluant agitation motrice), anxiété, nervosité, troubles du sommeil (insomnie) |
Affections du système nerveux : |
Fréquent : | céphalées, tremblements |
Très rare : | dysgueusie (altération du goût), sensations vertigineuses |
Affections cardiaques : |
Fréquent : | palpitations |
Peu fréquent : | tachycardie |
Rare : | arythmies (dont fibrillation auriculaire, tachycardie supraventriculaire, extrasystoles) |
Très rare : | angine de poitrine, allongement de l'intervalle QT, dèmes périphériques |
Affections vasculaires : |
Très rare : | variations de la pression artérielle |
Affections respiratoires, thoraciques et médiastinales : |
Peu fréquent : | bronchospasme, irritation de la gorge (avec toux et enrouement) |
Très rare : | bronchospasme paradoxal |
Affections gastro-intestinales : |
Peu fréquent : | sécheresse buccale |
Rare : | nausées |
Affections musculo-squelettiques et systémiques : |
Peu fréquent : | spasmes musculaires, myalgies |
Effets indésirables signalés avec l'utilisation de formotérol depuis sa commercialisation (fréquence indéterminée)
Les effets indésirables suivants ont été observés après commercialisation chez des patients traités avec formotérol. Ces effets indésirables ont été rapportés sous la forme de notifications spontanées, et sont présentés par classe de systèmes organes selon la classification MedDRA La version de MedDRA utilisée est la version 15.1. Au sein de chaque classe de systèmes organes, les événements indésirables sont présentés par ordre décroissant de fréquence (Tableau 2). Ces effets ayant été signalés spontanément par des personnes de la population générale (dont la taille n'est pas mesurable), il n'est pas toujours possible d'en évaluer correctement la fréquence.
Tableau 2. Effets indésirables rapportés de façon spontanée ou dans la littérature (fréquence indéterminée)
Troubles du métabolisme et de la nutrition : |
| augmentation des taux sanguins d'insuline, d'acides gras libres, de glycérol et des corps cétoniques |
Affections de la peau et du tissu sous-cutané : |
| rash |
Surdosage
Symptômes
L'expérience clinique de prise en charge d'un surdosage est limitée. Un surdosage de FORMOTÉROL risque d'entraîner les effets indésirables typiquement associés aux bêta‑2 mimétiques : céphalées, tremblements, palpitations. Dans des cas isolés, les événements suivants ont été rapportés : tachycardie, allongement de l'intervalle QTc, trouble du rythme (dont les arythmies ventriculaires), acidose métabolique, hypokaliémie, hyperglycémie, variation tensionnelle, hypertension, nausées et vomissements. Dans ces cas, un traitement d'appoint symptomatique est indiqué.
Traitement
Une surveillance est indiquée et un traitement d'appoint symptomatique doit être prescrit si nécessaire. Dans les cas les plus sévères, le patient pourra être hospitalisé.
Le recours à des bêta‑bloquants cardiosélectifs peut être envisagé mais uniquement sous surveillance médicale et avec prudence, l'utilisation de bêta‑bloquants pouvant provoquer un bronchospasme. La kaliémie doit être surveillée.
Grossesse/Allaitement
Femmes en âge de procréer
Il n'existe pas de recommandation particulière concernant les femmes en âge de procréer.
Grossesse
Les données concernant l'utilisation de formotérol chez la femme enceinte sont limitées. Un nombre limité d'études chez l'animal ne montre pas d'effets nocifs directs ou indirects de formotérol en termes de toxicité sur la reproduction .
Les études effectuées chez l'animal n'ont pas mis en évidence d'effet tératogène. En l'absence d'effet tératogène chez l'animal, un effet malformatif dans l'espèce humaine n'est pas attendu. En effet, à ce jour, les substances responsables de malformations dans l'espèce humaine se sont révélées tératogènes chez l'animal au cours d'études bien conduites sur deux espèces.
Il n'existe pas actuellement de donnés cliniques pertinentes sur un éventuel effet malformatif ou ftotoxique du formotérol lorsqu'il est administré pendant la grossesse.
Dans les études effectuées chez l'animal, l'utilisation de formotérol a provoqué des pertes embryonnaires lors de la nidation, a réduit la survie postnatale précoce et le poids à la naissance. Ces effets sont apparus pour des expositions systémiques nettement supérieures à celles atteintes aux posologies recommandées chez l'Homme.
Le formotérol, comme d'autres stimulants bêta‑2 adrénergiques, peut inhiber les contractions en fin de grossesse, en raison de son effet relaxant sur la musculature utérine lisse.
Quel que soit le stade de la grossesse, un traitement par FORMOTÉROL, peut être envisagé s'il est nécessaire pour obtenir le contrôle de l'asthme et si le bénéfice attendu pour la mère est supérieur au risque encouru par le ftus. Le risque potentiel d'utilisation chez l'homme n'est pas connu.
Allaitement
Les données concernant l'utilisation de formotérol chez la femme en période d'allaitement sont limitées. Chez l'Homme, le passage du formotérol dans le lait maternel n'est pas connu. Le formotérol a été retrouvé en petites quantités dans le lait de rates allaitantes . En conséquence et en raison du passage de nombreuses substances dans le lait maternel, l'utilisation de FORMOTÉROL au cours de l'allaitement ne doit être envisagée que si le bénéfice attendu pour la mère est supérieur au risque encouru par l'enfant.
Fertilité
Chez l'Homme, il n'y a pas de données disponibles concernant l'effet du formotérol sur la fertilité. Aucune altération de la fertilité n'a été observée dans des études menées chez des rats mâles et femelles .
Interactions avec d'autres médicaments
Les bêta‑bloquants peuvent diminuer ou inhiber l'effet du formotérol. FORMOTÉROL ne doit donc pas être utilisé en même temps que les bêta‑bloquants (même en collyres), sauf si nécessité absolue.
Aucune étude clinique spécifique n'a été menée pour étudier les interactions médicamenteuses avec le formotérol.
Un traitement concomitant avec d'autres agents sympathomimétiques tels que les autres bêta-2 sympathomimétiques ou l'éphédrine peut potentialiser les effets indésirables et nécessiter une diminution de la dose de FORMOTÉROL.
Un traitement concomitant par dérivés xanthiques, corticoïdes ou diurétiques tels que les thiazidiques ou les diurétiques de l'anse, peut potentialiser le risque d'effet indésirable rare d'hypokaliémie des bêta-2 agonistes . L'hypokaliémie est un facteur favorisant de l'arythmie cardiaque chez les patients traités par des glycosides digitaliques.
Il existe un risque théorique qu'un traitement concomitant avec d'autres substances connues pour prolonger l'intervalle QTc puisse entraîner une interaction pharmacodynamique avec le formotérol et augmenter le risque potentiel d'arythmie ventriculaire . En effet, l'action d'agonistes adrénergiques sur le système cardiovasculaire peut être potentialisée par exemple par les substances suivantes : certains antihistaminiques (comme la terfénadine, l'astémizole, la mizolastine) certains antiarythmiques (comme la quinidine, le disopyramide, le procainamide), les phénothiazines, les inhibiteurs de la monoamine oxydase, les macrolides (par exemple l'érythromycine) et les antidépresseurs tricycliques.
Le risque d'arythmie est augmenté chez les patients recevant un anesthésique volatil halogéné.
Les effets de FORMOTÉROL sur la bronchodilatation peuvent être augmentés par les agents anticholinergiques.

 Français
Français Русский
Русский